Бета Болезни повышен
Что такое Бета липопротеиды: норма для женщин и мужчин, причины повышения
Бета липопротеиды – липопротеины низкой плотности (ЛПНП), которые еще называют «плохим холестерином». Это наиболее атерогенный класс липопротеидов: высокий уровень ЛПНП связан с повышенным риском развития атеросклероза. Поэтому определение концентрации бета (б) липопротеидов имеет важное диагностическое значение.
Строение, функция липопротеидов низкой плотности
Бета липопротеиды – основная транспортная форма холестерина. Сам по себе стерол не растворяется водой. Поэтому чистый холестерол не может самостоятельно путешествовать по плазме крови. Для транспортировки синтезированный стерол связывается с липопротеинами очень низкой или низкой плотности. Последняя форма содержит гораздо больше стерола, чем первая.
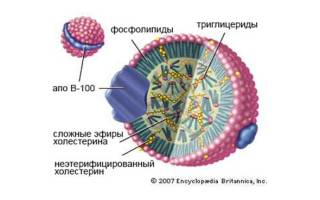
Структура бета (б) липопротеидов плазмы крови имеет следующий вид. Ядро ЛПНП образовано гидрофобным компонентом, преимущественно холестерином. Внешняя оболочка состоит из молекулы аполипопротеина B, фосфолипидов. От типа белка происходит второе название ЛПНП – бета липопротеиды. Аполипопротеин B стабилизирует молекулу липопротеида, а также является точкой прилипания к рецепторам-ЛПНП.
ЛПНП синтезируются печенью из липопротеинов очень низкой плотности, богатых триглицеридами. Процесс гидролиза сопровождается снижением концентрации триглицеридов, повышением уровня холестерина.
Размеры молекулы ЛПНП составляют 18-26 нм. Самые мелкие частицы (19-20,5 нм), называемые В-частицами, связаны с более высоким риском развития ишемической болезни сердца, кровоизлияния в головной мозг (инсульта). А-частицы или альфа более крупные (20,6-22 нм), не склонны оседать на стенках сосудов. Такую закономерность объясняют более легким проникновением мелких частиц в эндотелий артерий.
Бета липопротеиды в норме отвечают за доставку синтезированного холестерина от печени к тканям. Если какой-то клетке требуется стерол, она образует на своей поверхности ЛПНП-рецептор. Проплывающий мимо липопротеид начинает прилипать к нему аполипопротеином. Затем клетка поглощает ЛПНП, освобождает из него холестерин.
Недавние исследования показали, что бета-липопротеиды помогают организму противостоять инфицированию золотистым стафилококком. Механизм процесса до конца неясен, требует уточнения.
Норма липопротеидов для мужчин, женщин
Для бета липопротеидов норма изменяется с возрастом, зависит от пола. Взрослые мужчины имеют более высокий уровень холестерина-ЛПНП, чем женщины. С возрастом концентрация бета липопротеидов (ЛПНП) повышается.
| Возраст, лет | Пол | ЛПНП, ммоль/л |
|---|---|---|
| 5-10 | м | 1.64-3.35 |
| ж | 1.77-3.64 | |
| 10-15 | м | 1.67-3.45 |
| ж | 1.77-3.53 | |
| 15-20 | м | 1.62-3.38 |
| ж | 1.54-3.56 | |
| 20-25 | м | 1.72-3.82 |
| ж | 1.49-4.13 | |
| 25-30 | м | 1.82-4.28 |
| ж | 1.85-4.26 | |
| 30-35 | м | 2.03-4.78 |
| ж | 1.82-4.05 | |
| 35-40 | м | 2.11-4.91 |
| ж | 1.95-4.46 | |
| 40-45 | м | 2.26-4.83 |
| ж | 1.93-4.52 | |
| 45-50 | м | 2.52-5.24 |
| ж | 2.06-4.83 | |
| 50-55 | м | 2.32-5.11 |
| ж | 2.29-5.22 | |
| 55-60 | м | 2.29-5.27 |
| ж | 2.32-5.45 | |
| 60-65 | м | 2.16-5.45 |
| ж | 2.58-5.81 | |
| 65-70 | м | 2.55-5.45 |
| ж | 2.39-5.73 |
Уровень холестерола, ЛПНП зависит от физиологического состояния организма. Это касается женщин, поскольку у них наблюдаются циклические колебания концентрации гормонов, влияющих на уровень липопротеидов. На протяжении менструального цикла уровень холестерина, ЛПНП то повышается, то понижается.
Бета липопротеиды повышены при беременности. Особенно сильно концентрация ЛПНП, уровень холестерина повышается к третьему триместру. Это абсолютно нормальное явление, которое объясняется гормональной перестройкой организма.
Как контролировать уровень липопротеинов
Повышение бета-липопротеидов не сопровождается симптомами до тех пор, пока сформированная ими атеросклеротическая бляшка не перекроет значительно часть сосуда. Поэтому всем взрослым рекомендуется каждые 4-6 лет проверять уровень холестерина, ЛПНП, ЛПНОП, триглицеридов.
Больные сахарным диабетом, пациенты, имеющие высокое давление, наследственную предрасположенность к развитию ишемической болезни сердца, курящие находятся в группе повышенного риска. Им необходимо контролировать уровень фракций холестерина гораздо чаще.
Бета липопротеиды в крови определяются при помощи лабораторной диагностики. Для этого необходимо произвести забор крови из вены. Анализ на ЛПНП отдельно от других фракций липидов сдают редко. Обычно одновременно проверяют уровень холестерина, ЛПНП, ЛПНОП, триглицеридов. Такое комплексное исследование называют липидограммой.
Подготовка к забору крови
Анализ крови на бета липопротеиды не требует сложной подготовки. Необходимо соблюдать правила, общие для всех биохимических исследований:
- перед забором крови не кушать 12-14 часов. Из напитков разрешена только вода;
- исследование уровня бета липопротеидов проводится строго утром: с 8 до 10 часов;
- за сутки до сдачи липидограммы воздержитесь от спиртного, жирной пищи;
- за час до забора крови не курите, избегайте эмоциональных, физических нагрузок;
- непосредственно перед анализом посидите 5 минут.
Причины повышенного уровня
Повышенные бета липопротеиды могут быть симптомом заболевания или результатом нездорового образа жизни. Основные причины аномально высокого уровня ЛПНП:
- беременность (считается нормой);
- гиперлипопротеинемии 1А, 2В типов;
- диета, содержащая излишек холестерина, насыщенных жиров;
- заболевание почек (хроническая почечная недостаточность, нефротический синдром);
- закупорка желчевыводящих протоков;
- недостаточность щитовидной железы;
- нервная анорексия;
- ожирение;
- сахарный диабет;
- синдром Кушинга.
Повышенный уровень ЛПНП развивается на фоне приема диуретиков, бета-блокаторов, оральных контрацептивов, андрогенов, прогестинов, глюкокортикоидов.
Анализ Бета липопротеидов используют для определения степени риска сердечно-сосудистых осложнений атеросклероза: инфаркта миокарда, инсульта, ишемии. Высокие ЛПНП помогают обнаружить нарушения жирового обмена, когда до появления первых симптомов требуются годы.
Градация рисков, зависимо от концентрации ЛПНП.
| Концентрация | Степень риска | |
|---|---|---|
| мг/дл | ммоль/л | |
| менее 50 | менее 1,3 | Оптимальный уровень, низкий риск ишемической болезни сердца |
| 51-69 | 1,3-1,79 | Оптимальный уровень ЛПНП, при котором темпы прогрессирования атеросклероза минимальны. Такой уровень рекомендуется достигнуть людям, имеющим клиническую картину развития заболеваний. |
| 70-99 | 1,8-2,59 | Низкий уровень ЛПНП соответствует незначительной скорости прогрессирования атеросклероза. |
| 100-129 | 2,6-3,3 | Умеренный уровень ЛПНП, соответствующий высокой скорости развития атеросклероза. |
| 130-159 | 3,3-4,1 | Пограничный уровень ЛПНП, соответствующий среднему риску развития сердечно-сосудистых патологий. |
| 160-199 | 4,1-4,9 | Высокий уровень ЛПНП, связан с высоким риском развития осложнений. |
| более 200 | более 4,9 | Очень высокий риск. |
Причины пониженного уровня
При некоторых состояниях, заболеваниях уровень ЛПНП может быть понижен. Если соответствующий анализ крови выявил снижение ниже нормы бета липопротеидов, это говорит о:
- артритах;
- болезни Танжера;
- гиперфункции щитовидной железы;
- гипо-, а-бета-липопротеинемии;
- дефиците лецитинхолестеролацилсинетатазы;
- диете, содержащей недостаточное количество насыщенных жиров, холестерина;
- миеломной болезни;
- остром стрессе;
- синдроме мальабсорбции;
- синдроме Рейе;
- хронической анемии;
- хронических заболеваниях легких.
Бета липопротеиды бывают понижены на фоне приема холестирамина, неомицина, ловастатина, тироксина, интерферона, эстрогенов.
Профилактика
Повышение уровня ЛПНП можно избежать, если придерживать простых правил:
- Следить за питанием. Основу рациона должны составлять каши, овощи, фрукты, бобовые. Их дополняют рыбой, нежирными молочными продуктами, яйцами. А вот потребление красного мяса ограничивают, фаст-фуд – исключают.
- Отказаться от курения. Сигареты повышают уровень плохого холестерина, снижают концентрацию хорошего. Поэтому курильщики находятся в группе риска;
- Уделять физическим упражнениям не менее 30 минут/день. Они помогают поддерживать здоровый вес, снимают нагрузку с сердца, укрепляют сосуды, нормализируют уровень холестерина;
- Следите за своим весом. Избыточная масса тела часто связана с патологическим содержанием жиров плазмы крови, хроническими заболеваниями, включая повышенное давление;
- Необходимо регулярно сдавать анализ на холестерин, ЛПНП, ЛПОНП, триглицериды. Нормальным показателем считается контроль уровня жировых фракций каждые 4-6 лет.
Людям, склонным к развитию атеросклероза необходимо быть более внимательным к своему здоровью. Регулярные осмотры, соблюдение рекомендаций врача помогут сохранить здоровье максимально долгое время, вовремя заметить ухудшение самочувствия, принять меры.
Анализ на бета-2-микроглобулин
Что такое бета-2-микроглобулин?
Этот показатель часто используется в онкогематологии, то есть в разделе медицины, посвящённом онкологической патологии системы кроветворения, а также в нефрологии в качестве раннего показателя повреждения проксимальных канальцев почек. Соответственно, этот маркер можно исследовать в крови и в моче.
Бета-2-микроглобулин — белок, относящийся к комплексу лейкоцитарного антигена человека (HLA), молекулы которого имеются на большинстве клеток человеческого организма. Этот белок связан с расположенными рядом молекулами альфа-1 и альфа-3, и вместе они относятся к главному комплексу гистосовместимости 1 класса (МНС 1), которого нет только на эритроцитах и клетках трофобласта.
Вторым важным моментом является вопрос выведения белка из организма. Время жизни бета-2-микроглобулина — около 3,5 часов, соответственно в норме он активно нарабатывается и активно элиминируется почками. Если утилизировать белок из плазмы возможности нет и показатели почечного клиренса уменьшились, можно заподозрить патологию фильтрующего аппарата почек, что важно в сфере нефрологии и трансплантологии.
Нормальные значения показателя
Нормальная концентрация бета-2-микроглобулина в крови коррелирует с возрастом человека. У детей первого полугодия жизни отмечается довольно высокая норма этого белка: в среднем — 1,6-4 мг/л. В возрасте 6-12 месяцев показатель снижается до 0,8-2,5 мг/л. У детей до 7 лет уровень белка держится на достаточно стабильном уровне 0,7-2,3 мг/л, после чего идёт на убыль — 0,6-1,7 мг/л. Для лиц, старше 18 лет нормой считается показатель 0,67-2,3 мг/л.
Уровень бета-2-микроглобулина в моче более стабильный — менее 0,3 мг/л независимо от возраста.
Повышение показателя: причины, признаки и симптомы
Повышение значений бета-2-микроглобулина в крови обычно свидетельствует об одном из процессов:
- Опухолевые поражения органов кроветворной системы, лимфопролиферативные процессы. Наиболее частые заболевания — лимфоцитарный лейкоз, миеломная болезнь, лимфома Ходжкина, неходжкинская лимфома.
- Аутоиммунные процессы, связанные с агрессивным действием иммунных клеток на ткани и органы самого больного. Этиология, как правило, не известна. Предрасполагающими факторами считаются генетические мутации, наследственная предрасположенность, действие генома вирусов на клетки человека. Наиболее частые болезни: системная красная волчанка, синдром Шегрена, системная склеродермия, ревматоидный артрит.
- Вирусные заболевания, для которых характерна пожизненная персистенция вируса в организме человека. Например, ВИЧ, цитомегаловирус, вирус Эпштейна-Барр. Перечисленные инфекционные агенты разрушают клетки лимфоидного ряда, в результате чего концентрация содержащегося в них белка увеличивается в сыворотке крови.
- Поражения почек: отторжение трансплантата, ХБП, люпус-нефрит, инфекции, токсины.
Повышение значений бета-2-микроглобулина в моче может быть в двух случаях:
- Патология почек, при которой нарушается нормальный процесс фильтрации мочи в проксимальных извитых канальцах почек, не происходит обратное всасывание молекул белка, что приводит к избыточному удалению его с мочой.Примерный диагностический ряд:
- нарушение функции почечного трансплантата;
- тяжёлая диабетическая нефропатия;
- аутоиммунное поражение почек, например, при СКВ;
- инфекционный процесс верхних отделов мочевыводящих путей;
- интоксикация химикатами, лекарствами (антибиотики, препараты платины, контрастные вещества, цитостатики), тяжёлыми металлами (ртуть, кобальт, свинец, кадмий).
Симптомы и признаки зависят от конкретной патологии.
Например, при поражении почек, часто отмечается отёчный синдром с преимущественными отёками лица, может быть учащено, либо уменьшено мочеиспускание, моча может быть мутной, тёмной или осветлённой, иногда она приобретает нехарактерный запах. Нередко у пациента возникают боли в поясничной области, может появляться лихорадка, ознобы. В анализах крови важно отслеживать показатели эритроцитов, лейкоцитов, СОЭ, СРБ, креатинина, мочевины, электролитов.
В случае гематологических заболеваний, например, лимфобластного лейкоза, пациента беспокоит интоксикационный сидром, анемия, тромбоцитопения, увеличение размеров печени, селезёнки и т.д. В случае миеломной болезни наблюдается разрушение костей, часто — черепа, позвонков. Поражаются почки, возникают симптомы анемии, в крови увеличен уровень кальция, парапротеин сыворотки. В случае онкогематологических заболеваний наиболее информативный показатель — цитологическая картина костного мозга.
Снижение показателя: причины, признаки и симптомы
Особой диагностической ценности снижение показателя в крови не несёт, оно встречается в случае
- успешного лечения онкогематологических заболеваний;
- при усиленном выведении белка с мочой (следует дообследовать почки).
Низкий показатель бета-2-микроглобулина в моче (вплоть до 0 мг/л) является нормой.
Показания к проведению исследования
- Подозрение на онкогематологический процесс в организме (лейкозы, лимфомы, миеломная болезнь).
- Подозрение на аутоиммунный процесс в организме, оценка активности заболевания.
- Патологические процессы в почках:
- при хронической почечной недостаточности вследствие аутоиммунных процессов, сахарного диабета, сосудистой патологии почек;
- при интоксикации вследствие действия тяжёлых металлов (кадмий, ртуть, свинец), химических соединений, в том числе — лекарств;
- контроль состояния почки после её трансплантации;
- при сложностях в локализации инфекционного процесса в мочевыделительной системе (отличия воспаления верхних и нижних мочевыводящих путей).
Подготовка к анализу
Данный анализ обычно не требует тщательной предварительной подготовки. Рекомендации перед анализом крови универсальные:
- желательно сдавать кровь утром натощак (после ночного голодания 8-10 часов), либо в любое время суток не ранее, чем через 4 часа после последнего приёма пищи;
- до исследования можно пить воду в умеренном количестве, но с чаем, кофе, газировкой и алкоголем лучше повременить;
- накануне исследования (за 2-3 дня) избегать крайностей — пищевых перегрузок калорийной пищей и голода;
- не курить за 30-60 минут до анализа;
- желательно ограничить тяжёлые физические, психические нагрузки и физиопроцедуры за 1-2 дня до анализа;
- лекарственные препараты, не являющиеся жизненно важными для пациента, также рекомендуется отменить за 2-3 дня до исследования.
Расшифровка результатов теста
Лаборатория выдаёт заключение о концентрации белка в крови или в моче. Обычно в заключении указываются нормальные референсные значения, единица измерения, принятая в данной лаборатории (чаще — мг/л), а также показатели бета-2-микроглобулина у конкретного пациента. Клинических заключений лаборатория не даёт, но может перечислить ряд патологий, при которых результат может быть повышен.
Клинический диагноз может установить только врач гематолог, нефролог или другой врач, компетентный в данной сфере. Для установления конкретного диагноза одного анализа на бета-2-микроглобулин, как правило, мало, он входит в большой диагностический комплекс, в котором могут быть общие анализы крови и мочи, биохимические анализы, анализы пункционной биопсии костного мозга, лимфоузлов, визуализирующие методы исследования (УЗИ, рентгенография, КТ, МРТ) и многие другие.
Что может повлиять на результат?
- Неправильная подготовка.
- Проведение исследования без учёта принимаемых лекарств.
- Неисправность техники в лаборатории.
Коррекция показателей
Коррекция уровня бета-2-микроглобулина происходит в случае лечения пациента от основного патологического процесса в организме. Например, от онкогематологических заболеваний лечат в стационарных условиях, применяя длительную химиотерапию, во время которой можно использовать показатель бета-2-микроглобулина для отслеживания динамики и уменьшения лимфоидной пролиферации в организме.
Бета-талассемия
Талассемия — группа тяжелых генетических заболеваний крови, при которых нарушается синтез жизненно важного белка гемоглобина, входящего в состав эритроцитов, обеспечивающих кислородом все ткани и органы. Болезнь развивается из-за нарушения синтеза гемоглобина, связанного со сниженной продукцией одной из полипептидных цепей глобина (альфа, бета,гамма, дельта). Если нарушается синтез альфа-глобиновых цепей, болезнь классифицируют как альфа-талассемию. В случае недостаточного синтеза бета-глобиновых пептидных цепей, патологию определяют как бета-талассемию.
Заболеваемость альфа-талассемией распространена в южно-азиатских и западноафриканских странах. Бета-талассемия чаще встречается в Средиземноморских регионах, а также станах Северной Африки западной Азии. Ежегодно по всему миру рождается более 280 тысяч детей с синдромом талассемии.
Если вам необходима консультация специалиста по орфанным заболеваниям, заполнив все поля формы, и наши консультанты будут рады Вам помочь.
Что такое бета-талассемия
По данным ВОЗ, бета-талассемия является наиболее распространенной формой из группы наследственных заболеваний крови по аутосомно-рецессивному типу. В равной степени затрагивает как женщин, так и мужчин. Болезнь дифференцируют на гомозиготную форму, когда генетически она наследуется от одного из родителей и гетерозиготную форму, в случае наследования мутантного гена от обоих родителей.
Основная причина возникновения заболевания — мутации гена, который отвечает за синтез полипептидной цепи гемоглобина. Дефект на молекулярном уровне обусловлен неэффективным процессом или мутацией регуляторных генов, соединением аномальной матричной РНК или хромосомные перестройки структурных генов.
Механизм развития бета-талассемии заключается в недостаточном количестве синтезируемых бета-цепей, что приводит к избыточному продуцированию альфа-цепей, которые откладываются в клетках эритроидного ряда и повреждают их. Процесс сопровождается гибелью ретикулоцитов в селезенке, разрушением эритроцитов и деструкцией эритробластов в костном мозге, а также накоплением фетального гемоглобина. В результате этого сокращается транспортировка кислорода по всем тканям и органам, возникает хроническая анемия и тканевая гипоксия, что в свою очередь становится причиной многих заболеваний, в том числе костных деформаций и т.д.
МКБ-10
В класс МКБ-10 входят заболевания крови и кроветворных органов, а также гемолитические анемии, талассемии и тяжелая бета-талассемия (анемия Кули). По международной классификации болезней из группы МКБ-10, бета-талассемии присвоен код D56.1.
Симптомы
Клиническая картина при бета-талассемии проявляется у детей в течение 1-2 лет после рождения. Гомозиготная форма болезни сопровождается слабостью, хронической усталостью, повышением температуры тела, одышкой, бледностью и желтушностью кожного покрова, интоксикацией. Вследствие хронической анемии у детей наблюдается значительная задержка в физическом и умственном развитии. Нередко при бета-талассемии обнаруживаются нарушения в работе сердца, печени, эндокринных желез, что вызвано патологическим накоплением железа в организме. Из-за экстрамедуллярного кроветворения и тотального разрушения эритроцитов увеличивается селезенка и печень.
На фоне поражения трубчатых костей возникают патологические переломы, развивается синовит крупных суставов, желчнокаменная болезнь. Пациенты с бета-талассемией подвержены частым инфекционным болезням. Гомозиготная форма может привести к серьезным осложнениям: кардиосклерозу, сахарному диабету, сердечной недостаточности, циррозу печени, сепсису, пневмонии.
Бета-талассемия гетерозиготной формы может протекать бессимптомно или с незначительными проявлениями: повышенной утомляемостью на фоне гипохромной анемии, головокружениями, небольшим увеличением селезенки, головными болями.
Признаки
Уже в первый год после рождения, у детей с большой бета-талассемией можно отметить внешние признаки заболевания. Это монголоидный овал лица, характерный разрез глаз, четырехугольная (башенная) форма черепа, расширенная носовая перегородка (седловидная переносица), увеличенная верхняя челюсть, неправильный прикус. Наблюдается изменения скелетной структуры, иногда могут образовываться изъязвления в области голеней на фоне желтушности кожи. У маленьких детей достаточно выраженные внешние признаки бета-талассемии, что дает основания для предварительного диагноза.
Диагностика
При подозрениях на бета-талассемию специалисты в первую очередь изучают семейный анамнез, учитывают жалобы пациента и проводят физикальный осмотр. Для постановки диагноза требуется комплексное обследование, состоящее из таких процедур:
- Лабораторные исследования крови, позволяющие определить уровень железа, концентрацию билирубина, средний объем эритроцитов, нарушения цепей гемоглобина и другие показатели.
- Молекулярно-генетические исследования на предмет генных мутаций.
- Пункция костного мозга, подтверждающая гиперплазию красного кроветворного ростка.
- Краниография черепа, выявляющая игольчатый периостоз (симптом волосатого черепа).
- УЗИ брюшной полости — для оценки состояния желчевыводящих путей, а также размеров печени и селезенки.
В процессе обследования бета-талассемию дифференцируют от аутоиммунной, железодефицитной и серповидно-клеточной анемии, а также от наследственного микросфероцитоза. Немаловажное значение имеет пренатальная диагностика. Женщинам, у которых в семье есть родственники с подобным диагнозом, необходимо провести забор амниотической жидкости, чтобы подтвердить или опровергнуть наличие генетической патологии у плода. Данное исследование позволит начать своевременное лечение.
Классификация
В зависимости от генетических факторов и степени тяжести симптоматической картины, бета-талассемию разделяют на 3 группы:
Малая бета-талассемия — легкая форма заболевания, когда полной или частичной мутации подвержен только 1 ген, отвечающий за синтез бета-цепей. В анамнезе у носителей этой формы болезни отмечается лишь небольшой уровень эритроцитов в крови и легкая степень анемии.
Большая бета-талассемия — тяжелая форма патологии, при которой мутация затрагивает оба гена, ответственных за синтез полипептидных цепей гемоглобина. При большой бета-талассемии у детей до года, существует высокий риск летального исхода.
Промежуточная бета-талассемия — отличается большим дефицитом бета-цепей, может переходить в тяжелую форму болезни. В большинстве случаев протекает без серьезных нарушений в организме с минимально выраженной клинической картиной.
Лечение бета-талассемии
Тактика лечения зависит от формы и степени тяжести талассемии. Пациенты с малой бета-талассемией в лечении не нуждаются и могут самостоятельно компенсировать последствия врожденного заболевания, соблюдая здоровый образ жизни (отказ от вредных привычек, двигательная активность, сбалансированное питание).
При большой и промежуточной бета-талассемии врачи применяют следующие методы лечения:
- Трансфузионная терапия — переливание донорской крови. В случае промежуточной формы бета-талассемии трансфузию проводят редко, при сердечной недостаточности, легочной гипертензии, тяжелых костных деформациях, значительной задержке роста. Большая форма заболевания требует регулярного переливания эритроцитов (1-2 раза в месяц).
- Хелаторная терапия — введение препаратов, связывающих железо и выводящих его из организма. При гемолитических кризах используют глюкокортикоиды.
- Спленэктомия — удаление селезенки в случае ее гипертрофии.
- Пересадка костного мозга (ТКМ) — трансплантация донорских стволовых клеток, способствует возобновлению нормальной работы кроветворной системы.
Также пациентам со всеми формами бета-талассемии показан прием витаминов В, С, Е и фолиевой кислоты. Для предотвращения инфекционных осложнений требуется вакцинация.
Прогноз заболевания и профилактика
После пересадки костного мозга многие пациенты полностью выздоравливают. Постоянное переливание эритроцитной массы увеличивает продолжительность жизни маленьким детям, у которых была выявлена большая бета-талассемия. При гетерозиготной форме заболевания с бессимптомным течением качество и продолжительность жизни не страдают.
Профилактика бета-талассемии заключается в планировании беременности будущих родителей. Супружеской паре необходимо обязательно проконсультироваться с генетиком, если у кого-то из родственников была выявлена анемия Кули. При высоком генетическом риске носители мутантных генов должны отказаться от деторождения. Также к первичной профилактике бета-талассемии относят дородовую диагностику плода.
Если вам необходима консультация специалиста по орфанным заболеваниям, заполнив все поля формы, и наши консультанты будут рады Вам помочь.
Бета-талассемия
Талассемия — группа тяжелых генетических заболеваний крови, при которых нарушается синтез жизненно важного белка гемоглобина, входящего в состав эритроцитов, обеспечивающих кислородом все ткани и органы. Болезнь развивается из-за нарушения синтеза гемоглобина, связанного со сниженной продукцией одной из полипептидных цепей глобина (альфа, бета,гамма, дельта). Если нарушается синтез альфа-глобиновых цепей, болезнь классифицируют как альфа-талассемию. В случае недостаточного синтеза бета-глобиновых пептидных цепей, патологию определяют как бета-талассемию.
Заболеваемость альфа-талассемией распространена в южно-азиатских и западноафриканских странах. Бета-талассемия чаще встречается в Средиземноморских регионах, а также станах Северной Африки западной Азии. Ежегодно по всему миру рождается более 280 тысяч детей с синдромом талассемии.
Если вам необходима консультация специалиста по орфанным заболеваниям, заполнив все поля формы, и наши консультанты будут рады Вам помочь.
Что такое бета-талассемия
По данным ВОЗ, бета-талассемия является наиболее распространенной формой из группы наследственных заболеваний крови по аутосомно-рецессивному типу. В равной степени затрагивает как женщин, так и мужчин. Болезнь дифференцируют на гомозиготную форму, когда генетически она наследуется от одного из родителей и гетерозиготную форму, в случае наследования мутантного гена от обоих родителей.
Основная причина возникновения заболевания — мутации гена, который отвечает за синтез полипептидной цепи гемоглобина. Дефект на молекулярном уровне обусловлен неэффективным процессом или мутацией регуляторных генов, соединением аномальной матричной РНК или хромосомные перестройки структурных генов.
Механизм развития бета-талассемии заключается в недостаточном количестве синтезируемых бета-цепей, что приводит к избыточному продуцированию альфа-цепей, которые откладываются в клетках эритроидного ряда и повреждают их. Процесс сопровождается гибелью ретикулоцитов в селезенке, разрушением эритроцитов и деструкцией эритробластов в костном мозге, а также накоплением фетального гемоглобина. В результате этого сокращается транспортировка кислорода по всем тканям и органам, возникает хроническая анемия и тканевая гипоксия, что в свою очередь становится причиной многих заболеваний, в том числе костных деформаций и т.д.
МКБ-10
В класс МКБ-10 входят заболевания крови и кроветворных органов, а также гемолитические анемии, талассемии и тяжелая бета-талассемия (анемия Кули). По международной классификации болезней из группы МКБ-10, бета-талассемии присвоен код D56.1.
Симптомы
Клиническая картина при бета-талассемии проявляется у детей в течение 1-2 лет после рождения. Гомозиготная форма болезни сопровождается слабостью, хронической усталостью, повышением температуры тела, одышкой, бледностью и желтушностью кожного покрова, интоксикацией. Вследствие хронической анемии у детей наблюдается значительная задержка в физическом и умственном развитии. Нередко при бета-талассемии обнаруживаются нарушения в работе сердца, печени, эндокринных желез, что вызвано патологическим накоплением железа в организме. Из-за экстрамедуллярного кроветворения и тотального разрушения эритроцитов увеличивается селезенка и печень.
На фоне поражения трубчатых костей возникают патологические переломы, развивается синовит крупных суставов, желчнокаменная болезнь. Пациенты с бета-талассемией подвержены частым инфекционным болезням. Гомозиготная форма может привести к серьезным осложнениям: кардиосклерозу, сахарному диабету, сердечной недостаточности, циррозу печени, сепсису, пневмонии.
Бета-талассемия гетерозиготной формы может протекать бессимптомно или с незначительными проявлениями: повышенной утомляемостью на фоне гипохромной анемии, головокружениями, небольшим увеличением селезенки, головными болями.
Признаки
Уже в первый год после рождения, у детей с большой бета-талассемией можно отметить внешние признаки заболевания. Это монголоидный овал лица, характерный разрез глаз, четырехугольная (башенная) форма черепа, расширенная носовая перегородка (седловидная переносица), увеличенная верхняя челюсть, неправильный прикус. Наблюдается изменения скелетной структуры, иногда могут образовываться изъязвления в области голеней на фоне желтушности кожи. У маленьких детей достаточно выраженные внешние признаки бета-талассемии, что дает основания для предварительного диагноза.
Диагностика
При подозрениях на бета-талассемию специалисты в первую очередь изучают семейный анамнез, учитывают жалобы пациента и проводят физикальный осмотр. Для постановки диагноза требуется комплексное обследование, состоящее из таких процедур:
- Лабораторные исследования крови, позволяющие определить уровень железа, концентрацию билирубина, средний объем эритроцитов, нарушения цепей гемоглобина и другие показатели.
- Молекулярно-генетические исследования на предмет генных мутаций.
- Пункция костного мозга, подтверждающая гиперплазию красного кроветворного ростка.
- Краниография черепа, выявляющая игольчатый периостоз (симптом волосатого черепа).
- УЗИ брюшной полости — для оценки состояния желчевыводящих путей, а также размеров печени и селезенки.
В процессе обследования бета-талассемию дифференцируют от аутоиммунной, железодефицитной и серповидно-клеточной анемии, а также от наследственного микросфероцитоза. Немаловажное значение имеет пренатальная диагностика. Женщинам, у которых в семье есть родственники с подобным диагнозом, необходимо провести забор амниотической жидкости, чтобы подтвердить или опровергнуть наличие генетической патологии у плода. Данное исследование позволит начать своевременное лечение.
Классификация
В зависимости от генетических факторов и степени тяжести симптоматической картины, бета-талассемию разделяют на 3 группы:
Малая бета-талассемия — легкая форма заболевания, когда полной или частичной мутации подвержен только 1 ген, отвечающий за синтез бета-цепей. В анамнезе у носителей этой формы болезни отмечается лишь небольшой уровень эритроцитов в крови и легкая степень анемии.
Большая бета-талассемия — тяжелая форма патологии, при которой мутация затрагивает оба гена, ответственных за синтез полипептидных цепей гемоглобина. При большой бета-талассемии у детей до года, существует высокий риск летального исхода.
Промежуточная бета-талассемия — отличается большим дефицитом бета-цепей, может переходить в тяжелую форму болезни. В большинстве случаев протекает без серьезных нарушений в организме с минимально выраженной клинической картиной.
Лечение бета-талассемии
Тактика лечения зависит от формы и степени тяжести талассемии. Пациенты с малой бета-талассемией в лечении не нуждаются и могут самостоятельно компенсировать последствия врожденного заболевания, соблюдая здоровый образ жизни (отказ от вредных привычек, двигательная активность, сбалансированное питание).
При большой и промежуточной бета-талассемии врачи применяют следующие методы лечения:
- Трансфузионная терапия — переливание донорской крови. В случае промежуточной формы бета-талассемии трансфузию проводят редко, при сердечной недостаточности, легочной гипертензии, тяжелых костных деформациях, значительной задержке роста. Большая форма заболевания требует регулярного переливания эритроцитов (1-2 раза в месяц).
- Хелаторная терапия — введение препаратов, связывающих железо и выводящих его из организма. При гемолитических кризах используют глюкокортикоиды.
- Спленэктомия — удаление селезенки в случае ее гипертрофии.
- Пересадка костного мозга (ТКМ) — трансплантация донорских стволовых клеток, способствует возобновлению нормальной работы кроветворной системы.
Также пациентам со всеми формами бета-талассемии показан прием витаминов В, С, Е и фолиевой кислоты. Для предотвращения инфекционных осложнений требуется вакцинация.
Прогноз заболевания и профилактика
После пересадки костного мозга многие пациенты полностью выздоравливают. Постоянное переливание эритроцитной массы увеличивает продолжительность жизни маленьким детям, у которых была выявлена большая бета-талассемия. При гетерозиготной форме заболевания с бессимптомным течением качество и продолжительность жизни не страдают.
Профилактика бета-талассемии заключается в планировании беременности будущих родителей. Супружеской паре необходимо обязательно проконсультироваться с генетиком, если у кого-то из родственников была выявлена анемия Кули. При высоком генетическом риске носители мутантных генов должны отказаться от деторождения. Также к первичной профилактике бета-талассемии относят дородовую диагностику плода.
Если вам необходима консультация специалиста по орфанным заболеваниям, заполнив все поля формы, и наши консультанты будут рады Вам помочь.
Что такое глобулин?
Глобулин — это белок крови, важный для регуляции работы наших организмов. Зачем нужны глобулины?
- переносят гормоны, витамины и другие вещества;
- защищают организм от вирусов, бактерий, токсинов, чужеродных белков, вырабатывая на них антитела;
- регулируют свертываемость крови;
- связывают половые гормоны, лекарства, углеводы и другие вещества.
Количество глобулинов может отклоняться от нормы в таких случаях:
- воспалительный процесс;
- нарушения в работе печени, почек, легких, эндокринной системы;
- гормональные изменения;
- физические или химические повреждения органов;
- онкологическое заболевание;
- ВИЧ-инфекция;
- преклонный возраст (у мужчин может быть повышена концентрация глобулинов).
Количество глобулинов регулируют половые гормоны: эстрогены повышают их уровень, андрогены — понижают. Соответственно, у женщин глобулины крови содержатся в большем количестве, чем у мужчин.
Глобулин, связывающий половые гормоны
Печень вырабатывает большинство белков крови, среди которых ГСПГ — глобулин, связывающий половые гормоны . Чтобы организм правильно работал, часть гормонов должна быть связана. Связанный гормон неактивен, в то время как свободный активен и выполняет все свои функции. Связывая «лишние» гормоны, белок ограничивает их влияние на организм.
ГСПГ связывает прогестерон, эстрадиол, тестостерон, андростендион, 5-дигидротестостерон. Когда уменьшается количество ГСПГ, повышается концентрация активных (свободных, несвязанных) гормонов. При увеличенном количестве несвязанных половых гормонов может наблюдаться нерегулярный менструальный цикл и рост волос на лице (у женщин), увеличение молочных желез (у мужчин) и другие эффекты.
Если вы подозреваете, что у вас глобулин повышен или понижен, посоветуйтесь с врачом. Он выпишет направление на анализ ГСПГ. Женщины могут сдавать его в любой день менструального цикла.
ГСПГ: норма
У женщин репродуктивного возрастаглобулин, связывающий половые гормоны, должен быть в концентрации 26,1–110,0 нмоль/л.
У женщин в период постменопаузы— 14,1–68,9 нмоль/л.
У мужчин их уровень должен быть в пределах 14,5–48,4 нмоль/л.
Глобулин повышен — возможные причины:
- увеличенное количество эстрогенов;
- нарушения функции эндокринной системы;
- гепатит;
- ВИЧ-инфекция;
- прием оральных контрацептивов.
Пониженному уровню ГСПГ способствуют:
- увеличенный уровень гормонов (тестостерона, кортизола, пролактина);
- гигантизм;
- синдром поликистозных яичников;
- цирроз печени;
- нефротический синдром;
- недостаточное количество гормонов щитовидной железы;
- синдром недостаточной восприимчивости клеток к инсулину.
Глобулины — группа белков, включающая несколько подгрупп: альфа-1, альфа-2, бета и гамма. Их количество колеблется во время заболеваний.
Фракции (группы) глобулинов
Острые воспалительные процессы
Острые вирусные и бактериальные заболевания, инфаркт миокарда, ранние стадии пневмонии, острые полиартриты, туберкулез (экссудативный)
Хронические воспалительные процессы
Холецистит, пиелит, цистит, поздние стадии пневмонии, хронические туберкулез и эндокардит
Нарушения функции почек
Нефрит, токсикоз во время беременности, туберкулез (терминальные стадии), нефросклероз, нефрит, кахексия
Опухоли в различных органах с метастазами
Отравления печени, гепатит, лейкемия, онкология лимфатического и кроветворного аппарата, дерматоз, полиартрит (некоторые формы)
Тяжелые формы туберкулеза, хронический полиартрит и коллагеноз, цирроз печени
Рак желчевыводящих путей и головки поджелудочной железы, а также обтурационная желтуха
↑ — означает, что концентрация растет
↓—означает, что концентрация снижается
Альфа-глобулины
Альфа-глобулины подразделяют на две категории: альфа-1-глобулины и альфа-2-глобулины.
Норма альфа-1-глобулинов составляет 3–6%, или 1–3 г/л.
Среди альфа-1-глобулинов выделяют:
- альфа-1-антитрипсин;
- альфа-1-липопротеин;
- альфа-1-гликопротеин;
- альфа-1-фетопротеин;
- альфа-1-антихимотрипсин.
Эти вещества также называют белками острой фазы: они вырабатываются в увеличенных количествах при различных повреждениях органов (химических или физических), при вирусных и бактериальных инфекциях. Они останавливают дальнейшее повреждение тканей и не дают размножаться патогенным микроорганизмам.
Уровень альфа-1-глобулинов повышается при:
- вирусной и бактериальной инфекции;
- остром и хроническом воспалении;
- злокачественной опухоли;
- повреждении кожи (ожоге, травме);
- отравлении;
- изменении гормонального фона (терапии стероидами, беременности);
- системной красной волчанке;
- повышении температуры тела;
- артрите;
- многоплодной беременности;
- пороках развития плода или его смерти.
Понижается уровень альфа-1-глобулинов, когда нарушена работа:
- легких (эмфизема);
- печени (цирроз, рак);
- почек (нефротический синдром);
- яичек (рак) и при онкологии других органов.
Их концентрация в норме составляет от 9 до 15% (6–10 г/л).
Среди альфа-2-глобулинов выделяют:
- альфа-2-макроглобулин;
- гаптоглобин;
- церулоплазмин;
- антиотензиноген;
- альфа-2-гликопротеин;
- альфа-2- HS-гликопротеин;
- альфа-2-антиплазмин;
- белок А.
Среди веществ данной группы есть белки острой фазы, а также транспортные белки.
Количество альфа-2-глобулинов увеличивается при:
- поражении печени (циррозе, гепатите);
- повреждении тканей (ожоге, травмах);
- воспалении;
- некрозе тканей (отмирании);
- злокачественных опухолях (с метастазами);
- эндокринных заболеваниях (сахарный диабет, микседема);
- изменении гормонального фона (лечении стероидными гормонами, беременности);
- желтухе;
- аутоиммунном заболевании;
- нарушении в работе почек (нефротический синдром).
Концентрация альфа-2-глобулинов может быть понижена при:
- недостаточном количестве белка в еде;
- ревматическом полиартрите;
- малокровии;
- заболеваниях желудочно-кишечного тракта;
- недостаточном питании;
- нарушении всасывания в кишечнике.
Бета-глобулины
При достаточном уровне бета-глобулинов их концентрация должна быть в пределах 8–18% (7–11 г/л).
В категории бета-глобулинов различают:
- гемопексин;
- трансферрин;
- стероид-связывающий бета-глобулин;
- бета и пребета-липопротеины.
Большинство бета-глобулинов — это транспортные белки.
- дефиците железа;
- приеме гормональных контрацептивов;
- беременности;
- сахарном диабете;
- дистрофии;
- повышенном уровне эстрогенов.
Пониженный уровень бета-глобулинов — причины:
- воспаление:
- злокачественная опухоль;
- малокровие;
- заболевание печени;
- недостаточное количество белка в пище;
- нефротический синдром;
- увеличенный уровень гормонов (тестостерона, пролактина, глюкокортикоидов);
- синдром недостаточной восприимчивости клеток к инсулину;
- нарушения в работе гипофиза;
- нарушения функций эндокринной системы.
Гамма-глобулины
Если организм правильно функционирует и выделяет гамма-глобулины, норма их должна быть в пределах 15–25% (8–16 г/л). К этой группе белков относят защитные белки — иммуноглобулины (Ig). Часто их называют антителами. Среди них различают:
- иммуноглобулины G (IgG) — защищают от вирусов и бактерий. Переносятся в больших количествах через плаценту.
- иммуноглобулины A (IgA) — защищают слизистые поверхности дыхательной системы и кишечника. Находятся в слюне, слезах, женском молозиве.
- иммуноглобулины M (IgM) — обеспечивают первичный иммунитет: после рождения и до 9 месяцев их количество возрастает, а потом уменьшается. Восстанавливается после 20 лет.
- иммуноглобулины E (IgE) — вырабатывают антитела на аллергены.
- иммуноглобулины D (IgD) — регулируют работу других иммуноглобулинов.
Среди иммуноглобулинов выделяют также группу криоглобулинов. Эти белки растворяются при нагревании и выпадают в осадок при охлаждении сыворотки крови. У здоровых людей их нет. Чаще всего они появляются при ревматическом артрите и миеломной болезни, вирусных гепатитах В и С, аутоиммунных и прочих заболеваниях.
Повышенное содержание гамма-глобулинов называется гипергаммаглобулинемия. Наблюдается при усилении иммунных процессов. Причинами, по которым гамма-глобулины повышаются, могут быть:
- острое и хроническое инфекционное заболевание крови;
- некоторые опухоли;
- гепатит и цирроз печени.
Гамма-глобулины могут находиться в низкой концентрации при:
- слабом иммунитете;
- хроническом воспалительном процессе;
- аллергической реакции;
- длительном лечении стероидными гормонами;
- СПИДе.
Если человек переболел определенным заболеванием, то из его крови можно извлечь антитела к данной болезни — гамма-глобулины. Кроме этого, их можно получать из крови животных. Для этого животным (чаще всего лошадям) предварительно вводят специальную вакцину.
Для профилактики и лечения рекомендуют вводить гамма-глобулины сразу после контакта с зараженным больным или на ранних стадиях заболевания. Особенно это эффективно в первые два дня болезни.
Когда у человека в крови есть гамма-глобулины, болезнь проходит быстрее и снижается вероятность осложнений. На сегодняшний день выделены гамма-глобулины против гриппа, дизентерии, инфекционного гепатита, клещевого энцефалита, коклюша, кори, краснухи, оспы, свинки, сибирской язвы и скарлатины.
Гамма-глобулины матери в первые полгода жизни ребенка защищают его от заболеваний.