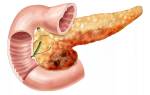
Гормоны поджелудочной железы биохимия
Гормоны поджелудочной железы
Гормонами поджелудочной железы являются инсулин и глюкагон.
Глюкагон
Строение
Представляет собой полипептид, включающий 29 аминокислот с молекулярной массой 3,5 кДа и периодом полураспада 3-6 мин.
Синтез
Осуществляется в клетках поджелудочной железы и в клетках тонкого кишечника.
Регуляция синтеза и секреции
Активируют : гипогликемия, адреналин.
Уменьшают : глюкоза, жирные кислоты.
Механизм действия
Мишени и эффекты
Конечным эффектом является повышение концентрации глюкозы и жирных кислот в крови.
Жировая ткань
- повышает активность внутриклеточной гормон-чувствительной ТАГ-липазы и, соответственно, стимулирует липолиз.
Печень
- активация глюконеогенеза и гликогенолиза,
- за счет повышенного поступления жирных кислот из жировой ткани усиливает кетогенез.
Патология
Гиперфункция
Глюкагонома – редко встречающееся новообразование из группы нейроэндокринных опухолей. У больных отмечается гипергликемия и поражение кожи и слизистых оболочек.
Инсулин
Строение
Представляет собой полипептид из 51 аминокислоты, массой 5,7 кД, состоящий из двух цепей А и В, связанных между собой дисульфидными мостиками.
Синтез
Синтезируется в клетках поджелудочной железы в виде проинсулина, в этом виде он упаковывается в секреторные гранулы и уже здесь образуется инсулин и С-пептид.
Регуляция синтеза и секреции
Активируют синтез и секрецию:
- глюкоза крови – главный регулятор, пороговая концентрация для секреции инсулина – 5,5 ммоль/л,
- жирные кислоты и аминокислоты,
- влияния n.vagus – находится под контролем гипоталамуса, активность которого определяется концентрацией глюкозы крови,
- гормоны ЖКТ: холецистокинин, секретин, гастрин, энтероглюкагон, желудочный ингибирующий полипептид,
- хроническое воздействие гормона роста, глюкокортикоидов, эстрогенов, прогестинов.
Уменьшают : влияние симпато-адреналовой системы.
Механизм действия
Осуществляется через рецепторы с тирозинкиназной активностью (подробно).
Мишени и эффекты
Основным эффектом является снижение концентрации глюкозы в крови благодаря усилению транспорта глюкозы внутрь миоцитов и адипоцитов и активации внутриклеточных реакций утилизации глюкозы:
- активируя фосфодиэстеразу, которая разрушает вторичный мессенджер цАМФ, инсулин прерывает эффекты адреналина и глюкагона на печень и жировую ткань.
- в мышцах и жировой ткани стимулирует транспорт глюкозы в клетки (активация Глют-4),
- в печени и мышцах ускоряет синтез гликогена (активация гликогенсинтазы).
- в печени, мышцах и адипоцитах инсулин стимулирует гликолиз, активируя фосфофруктокиназу и пируваткиназу.
- полученный в гликолизе пируват превращается в ацетил-SКоА под влиянием активированного инсулином пируватдегидрогеназного комплекса, и далее используется для синтеза жирных кислот. Превращение ацетил-SКоА в малонил-SКоА, первый субстрат синтеза жирных кислот, также стимулируется инсулином (ацетил-SКоА-карбоксилаза).
- в мышцах усиливает транспорт нейтральных аминокислот в миоциты и стимулирует трансляцию (рибосомальный синтез белков).
Ряд эффектов инсулина заключается в изменении транскрипции генов и скорости трансляции ферментов, отвечающих за обмен веществ, за рост и деление клеток.
Благодаря этому индуцируется синтез ферментов метаболизма
- углеводов в печени (глюкокиназа, пируваткиназа, глюкозо-6-фосфатдегидрогеназа),
- липидов в печени (АТФ-цитрат-лиаза, ацетил-SКоА-карбоксилаза, синтаза жирных кислот, цитозольная малатдегидрогеназа) и адипоцитах (ГАФ-дегидрогеназа, пальмитатсинтаза, липопротеинлипаза).
и происходит репрессия фосфоенолпируват-карбоксикиназы (подавление глюконеогенеза).
Инактивация инсулина
Инактивация инсулина начинается после интернализации инсулин-рецепторного комплекса и образования эндосомы, в которой и происходит деградация инсулина. Участвуют две ферментные системы:
- Глутатион-инсулин-трансгидрогеназа, которая восстанавливает дисульфидные связи между цепями А и В, в результате чего гормон распадается.
- Инсулиназа (инсулин-протеиназа), гидролизующая инсулин до аминокислот.
Период полужизни инсулина не превышает 5-6 минут. Происходит деградация в основном в печени и почках, но и другие ткани принимают в этом участие. Также в почках инсулин может фильтроваться, захватываться эпителиоцитами проксимальных канальцев и разрушаться до аминокислот.
Патология
Гипофункция
Инсулинзависимый и инсулиннезависимый сахарный диабет. Для диагностики этих патологий в клинике активно используют нагрузочные пробы и определение концентрации инсулина и С-пептида.
Развернутое лабораторное обследование поджелудочной железы
Комплексное исследование крови, которое позволяет выявить основные нарушения различной этиологии в функциональном состоянии поджелудочной железы.
Результаты исследований выдаются с бесплатным комментарием врача.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- Исключить из рациона алкоголь в течение 24 часов до исследования.
- Не принимать пищу в течение 12 часов до исследования, можно пить чистую негазированную воду.
- Исключить физическое и эмоциональное перенапряжение в течение 30 минут до исследования.
- Не курить в течение 3 часов до исследования.
Общая информация об исследовании
Поджелудочная железа – орган желудочно-кишечного тракта, расположенный позади желудка и выполняющий важные экзо- и эндокринные функции. Переваривание белков и жиров в тонкой кишке осуществляется благодаря синтезу и секреции ферментов пищеварения внешнесекреторной частью железы. Кроме протео- и липолитических ферментов она выделяет бикарбонаты, нейтрализуя соляную кислоту желудочного сока в двенадцатиперстной кишке. Эндокринная функция поджелудочной железы обеспечивается островковой тканью, в которой синтезируются и затем секретируются в кровь гормоны инсулин, глюкагон, соматостатин и панкреатический полипептид. Инсулин и глюкагон регулируют уровень глюкозы в крови и ее транспорт в тканях. Патология поджелудочной железы в первую очередь приводит к нарушению пищеварения, а при хронических заболеваниях способствует развитию эндокринных нарушений (сахарного диабета).
Причины заболеваний поджелудочной железы различны: генетические и аутоиммунные нарушения, инфекции (чаще вирусные), травмы, токсические поражения, прием некоторых лекарственных препаратов (эстрогенов, фуросемида, азатиоприна и др.), новообразования. Чаще всего патология поджелудочной железы возникает на фоне нарушений функции печени, заболеваний желчевыводящих путей (желчнокаменной болезни с холедохолитиазом), вследствие нарушения оттока желчи и поджелудочного сока. Еще одной распространенной причиной заболеваний поджелудочной является злоупотребление алкоголем.
Клинические проявления болезней поджелудочной железы зависят от этиологии, степени дисфункции и активности процесса. Острые воспалительные изменения, травма железы, а также хронические заболевания в период обострения в большинстве случаев сопровождаются болью и жжением в эпигастральной области с иррадиацией в спину, тошнотой, рвотой, повышением температуры тела. Хронические заболевания поджелудочной железы приводят к панкреатической недостаточности, потере веса, развитию асцита из-за нарушения переваривания и всасывания питательных веществ из кишечника.
Повышение в крови активности ферментов поджелудочной железы (амилазы и липазы) и уровня С-реактивного белка – признаки активного воспаления органа – острого панкреатита. Изменение уровня глюкозы и С-пептида указывает на нарушение эндокринной функции поджелудочной железы и является косвенным признаком повреждения панкреатической островковой ткани, которое может возникнуть при хроническом панкреатите. Резкое повышение онкомаркера СА 19-9 на фоне изменений биохимических показателей функции железы чаще всего свидетельствует о раке поджелудочной железы.
Увеличение концентрации ферментов амилазы и липазы свидетельствует об одновременном вовлечении в патологический процесс печени и поджелудочной железы, что обычно бывает при камне общего желчного протока и реактивном панкреатите.
При изменениях показателей данного комплексного анализа необходимо выполнить дополнительные лабораторные и инструментальные исследования для уточнения причин и механизмов развития заболевания, подбора терапии.
Для чего используется исследование?
- Для оценки функционального состояния поджелудочной железы и тяжести повреждения;
- для дифференциальной диагностики заболеваний поджелудочной железы;
- для наблюдения за пациентом с хроническими заболеваниями гепатопанкреабилиарной зоны (желчнокаменной болезнью, холелитиазом, хроническим панкреатитом);
- для контроля за эффективностью лечения заболеваний поджелудочной железы.
Когда назначается исследование?
- При симптомах вероятного поражения поджелудочной железы (опоясывающая боль и/или жжение в верхнем отделе живота, тошнота, рвота, изменение цвета, количества и консистенции стула);
- при изменении структуры и размеров поджелудочной железы по данным инструментальных методов исследования;
- при обследовании лиц, злоупотребляющих алкоголем;
- при наличии заболеваний поджелудочной железы в семейном анамнезе;
- при мониторинге пациентов с хроническими заболеваниями печени, поджелудочной железы и желчевыводящих путей;
- при профилактическом обследовании.
ГОРМОНЫ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
Поджелудочная железа расположена в брыжейке двенадцатиперстной кишки. Железа осуществляет две важнейшие функции: экзокринную и эндокринную. Большая ее часть (95%) выполняет экзокринную функцию — обеспечение синтеза и секреции пищеварительных ферментов. Эндокринная функция осуществляет секрецию гормонов, участвующих в регуляции различных процессов.
Для поджелудочной железы характерным является клеточный полиморфизм. Островки Лангерганса выделяют четыре типа клеток железы, каждый из которых вырабатывает определенный гормон: а-клетки (секретируют глюкагон), р-клетки (секретируют инсулин), D-клетки (секретируют соматостатин), F-клетки (секретируют панкреатический полипептид).
Уровень глюкозы в крови поддерживается сравнительно постоянным. Глюкоза в тканях трансформируется в глюкозо- 6-фосфат, ключевой посредник, который может быть направлен на синтез гликогена, синтез энергии по пути гликолиза, на окисление по пентозофосфатному пути. Судьба глюкозо-6-фос- фата определяется действием двух гормонов поджелудочной железы — инсулина и глюкагона. Высокий уровень глюкозы в крови приводит к увеличению секреции инсулина, а низкий уровень глюкозы стимулирует секрецию глюкагона.
Инсулин – это первый белковый гормон, полученный в 1925 г. в кристаллическом виде и с выясненной Сэнджером Ф. (Нобелевская премия, 1958, 1981) в 1953 г. аминокислотной последовательностью. М. м. инсулина = 5800. Он синтезируется в форме проинсулина (84 аминокислотных остатка), а затем в результате протеолиза в аппарате Гольджи с отщеплением С-пептида из 33 аминокислотных остатков переходит в активную форму. Таким образом, молекула инсулина состоит из двух полипептидных цепей (А и В) с 21 и 30 аминокислотами соответственно, связанных двумя дисульфидными связями. Из аппарата Гольджи инсулин поступает в везикулы, где связывается с цинком и депонируется в кристаллическом виде в секреторных гранулах (3-клеток.
Под влиянием различных стимулов инсулин освобождается от цинка и поступает по системе воротной вены в печень, где часть инсулина, не разрушенного в печени, остается в свободном виде. Из печени инсулин поступает в клетки-мишени. В крови инсулин не связан с транспортными белками, а поэтому его период полураспада составляет лишь 3-5 мин.
Главным биологическим стимулятором продукции инсулина является глюкоза, вступающая во взаимодействие с рецепторами плазматической мембраны (3-клеток. Связывание инсулина с его рецепторами на поверхности клеток-мишеней (печень, жировая ткань) без проникновения внутрь клетки вызывает образование в ней вторичных посредников, что приводит к активизации ферментов внутри клетки уже через несколько секунд или часов.
Механизм действия инсулина на обменные процессы детально еще не выяснен. При высоком содержании инсулина в крови число рецепторов гормона на поверхности мембран уменьшается и, таким образом, чувствительность тканей-мишеней к инсулину снижается. Жировая клетка, например, содержит 10 тыс. рецепторов, поэтому она более чувствительна к действию гормона, чем клетки печени.
Под влиянием притока к поджелудочной железе большого количества глюкозы секреция инсулина стимулируется: гли- когенсинтаза дефосфорилируется и становится активной, а глюкоза ориентируется на синтез гликогена. Стимуляторами секреции инсулина являются также АКТГ, СТГ, глюкокортикоиды, глюкагон, аминокислоты и другие биологически активные вещества. Соматостатин является ингибитором выделения инсулина. Кроме того, в регуляции секреции инсулина принимают участие парасимпатическая (стимулирует) и симпатическая (подавляет) нервная система. Важную роль в регуляции высвобождения гормона играет блуждающий нерв.
Инсулин — единственный гормон, способный понижать уровень сахара в крови, тогда как целый ряд других гормонов в организме повышает уровень сахара в крови. Во всех органах внутри клеток концентрация глюкозы ниже, чем вне клетки.
Инсулин облегчает диффузию глюкозы и аминокислот внутрь клеток, а в клетках печени способствует усилению фосфорилирования глюкозы. В результате фосфорилирования внутри клеток поддерживается низкий уровень свободной глюкозы, что усиливает приток глюкозы внутрь клеток. Внутри клеток инсулин усиливает гликолиз, синтез липидов, белков, гликогена, ингибирует липолиз. Все это приводит к снижению концентрации глюкозы в крови животного.
Инсулин — важнейший анаболический агент в печени, жировой ткани, мышцах. Эти эффекты объясняются усилением образования АТФ, НАДФН + Н + . Основной источник энергии в клетках — аэробный гликолиз, реакции которого активируются за счет влияния инсулина на клеточные ферменты этого процесса. Понижение в печени активности фермента фруктозо-1,6-дифосфатазы и пируваткарбоксилазы приводит к снижению глюконеогенеза.
Инсулин оказывает влияние на обмен липидов. Запасы липидов в организме увеличиваются за счет стимуляции транспорта глюкозы в клетки жировых депо, где глюкоза используется для синтеза триглицеридов. Инсулин ингибирует гормончувстви- тельную липазу, которая обеспечивает гидролиз триглицеридов жировых депо, в результате уровень жирных кислот в крови снижается.
После приема животным кормов инсулин усиливает синтез жирных кислот:
- • путем активации аэробного гликолиза и образования аце- тил-КоА митохондрий, что повышает концентрацию в цитоплазме цитрата и ацетил-КоА;
- • за счет прямой активации ацетил-КоА карбоксилазы, начального фермента синтеза жирных кислот;
- • за счет усиления образования НАДФН2 в пентозофосфат- ном пути.
Недостаток синтеза инсулина вызывает развитие в организме сахарного диабета (Diabetes mellitus) с признаками гипергликемии, глюкозурии, полиурии. Диабет характеризуется нарушениями метаболизма углеводов, жиров, белков. Гипергликемия при сахарном диабете связана с недостатком транспорта глюкозы внутрь клеток в силу снижения активности инсулина и высокой степени глюконеогенеза, так как действие глюкаго- на не сдерживается инсулином.
При инсулиновой недостаточности происходит усиление липолиза. Усиленный липолиз приводит к повышению уровня свободных жирных кислот и глицерина в крови и печени. Свободные жирные кислоты являются источником синтеза кетоновых тел, которые, накапливаясь, способствуют развитию ацидоза, усиливают тканевую гипоксию. Гепатоциты инфильтрируются продуктами жирового обмена, и создаются условия для развития жировой инфильтрации печени (диабетический стеатез).
При дефиците инсулина активируется глюконеогенез под действием глюкагона и гликогенолиз. Для синтеза глюкозы используются аминокислоты, образующиеся при усилении распада тканевых белков, в результате уровень белков в тканях снижается. В процессе глюконеогенеза активно используется аланин, поэтому в крови увеличивается содержание аминокислот с разветвленной цепью (валин, лейцин, изолейцин), утилизация которых мышечной тканью снижается. Таким образом, возникает гипергликемия и накопление продуктов распада белков — мочевины, азота, развивается гиперазотемия.
Инсулин также оказывает влияние на процессы репликации и транскрипции более чем 100 специфических мРНК в печени, сердечной и скелетных мышцах, жировой ткани, участвуя таким образом в клеточной пролиферации и дифференцировке. Инсулин ускоряет фосфорилирование белков, которые регулируют транспорт метаболитов и транскрипцию более 60 генов.
Вследствие гипергликемии происходит перераспределение воды в тканях, выход жидкости из клеток в кровяное русло, что приводит к тканевой дегидратации. Повышение уровня жирных кислот в печени вызывает усиление синтеза триглицеридов, липопротеинов, провоцируя ожирение печени.
В норме инсулин способствует транспорту аминокислот в клетки и синтезу белков. Однако у диабетиков повышение уровня аланина способствует усилению глюконеогенеза и гипергликемии. Повышение использования аминокислот приводит к увеличению синтеза мочевины в печени. В конечном счете усиление катаболизма аминокислот приводит к отрицательному азотистому балансу. При введении в организм инсулина указанные нарушения исчезают. При этом следует учитывать, что действие гормона по времени ограничено.
В настоящее время инсулин синтезирован химическим путем и методом генной инженерии. Препараты инсулина получают из поджелудочных желез свиней и крупного рогатого скота. По аминокислотному спектру из инсулинов животного происхождения наиболее близки к человеческому свиной и китовый инсулины, обладающие меньшей антигенной активностью. Человеческий инсулин впервые был получен в 1965 г., а его промышленный синтез осуществлен в 1980 г. Сегодня существуют два способа промышленного получения инсулина: биосинтетический и полусинтетический. Биосинтетический инсулин синтезирован путем генной инженерии (с использованием Е. coli), а полусинтетический препарат получают путем замены аланина в 30-ом положении В-полипептидной цепи молекулы инсулина свиньи на треонин.
По продолжительности действия инсулины подразделяются на инсулины короткого (6-8 ч), промежуточного (10-12 ч) и длительного действия (8-22 ч). К наиболее частым осложнениям, вызываемым введением инсулина, относятся гипогликемия, аллергические реакции. Явления гипогликемического шока наступают при снижении концентрации глюкозы в крови человека до 45-50 мг%.
Глюкагон – это полипептид, м. м. = 3600-4200, содержит 29 аминокислотных остатков. Синтезируется в а-клетках островков Лангерганса в форме проглюкагона в ответ на низкий уровень глюкозы в крови. В крови глюкагон не связан с белками- транспортерами и период его полураспада составляет 3-5 мин. Печень и почки быстро инактивируют глюкагон. Клетки печени — основные мишени глюкагона. Действие глюкагона прямо противоположно эффектам инсулина.
Первостепенное действие глюкагона — активация цАМФ- зависимой фосфорилазной системы печени с превращением гликогена в глюкозу, которая поступает в кровь. Клетки печени содержат фермент глюкозо-6-фосфорилазу и могут обеспечивать поступление свободной глюкозы в кровь. Мышечная и другие ткани имеют дефицит этого фермента, а поэтому не способны к «экспорту» глюкозы. Глюкагон также усиливает глюконеогенез в печени за счет активации ряда ферментов и увеличения в печени концентрации предшественников глюкозы.
Глюкагон снижает активность пируваткиназы и ацетил- КоА-карбоксилазы, стимулирует цАМФ-зависимую липазную активность в клетках жировой ткани, печени с превращением триглицеридов в свободные жирные кислоты и глицерин, что способствует усилению синтеза кетоновых тел. Таким образом глюкагон стимулирует липолиз.
Под влиянием глюкагона происходит угнетение синтеза белка и усиление его распада, поэтому значительная часть свободных аминокислот вовлекается в глюконеогенез. Высокое отношение глюкагон:инсулин в крови повышает уровень глю- конеогенеза и снижает активность гликолиза в печени. Низкое отношение глюкагон:инсулин имеет обратный эффект.
Соматостатин впервые выделен из гипоталамуса. Это циклический пептид из 14 аминокислотных остатков, синтезируемый также р-клетках поджелудочной железы в виде прогормона из 28 аминокислот. В настоящее время синтез сома- тостатина установлен и в разных отделах пищеварительного тракта.
Механизм действия соматостатина выяснен недостаточно. Вероятно, его эффекты связаны с блокированием поступления в клетки железы Са ++ , необходимого для секреции других гормонов поджелудочной железы. Соматостатин подавляет эффекты инсулина и глюкагона, тормозит секрецию гастрина и ферментов поджелудочной железы. Соматостатин снижает абсорбцию глюкозы в кишечнике, регулируя таким образом концентрацию сахара в крови. Соматостатин также блокирует высвобождение соматотропина гипофизом. Следует считать, что эффекты соматостатина проявляются не в подавлении синтеза других гормонов, а в торможении их секреции в кровь.
Панкреатический полипептид включает 36 аминокислотных остатков, м. м. = 4200, синтезируется F-клетками поджелудочной железы. Панкреатический полипептид способен расщеплять гликоген подобно глюкагону, активизировать ферменты поджелудочной железы и желудка. Можно полагать, что клетками-мишенями для этого гормона являются клетки всех отделов желудочно-кишечного тракта. Биохимические процессы, связанные с панкреатическим полипептидом, не изучены. При сахарном диабете выявлена гиперплазия синтезирующих полипептид клеток.
Гормоны поджелудочной железы: биохимия и синтез гликогена, функция ферментов
Все процессы в организме человека регулируются с помощью центральной нервной системы и гормонов, которые вырабатываются эндокринными органами. Отлаженные механизм позволяет быстро адаптироваться к внешним и внутренним негативным факторам.
Поджелудочная железа – уникальный орган, которые принимает не только участие в процессах пищеварения, но и предстает своеобразной «фабрикой», синтезирующей необходимые вещества для нормальной жизнедеятельности.
Внутренний орган состоит из эндокринной части, которая способствует продуцированию ферментов пищеварения и панкреатических островков, где синтезируются гормоны поджелудочной железы. Они помогают регулировать углеводный, белковый и жировой обмен.
Даже незначительный сбой в функционировании органа может привести к серьезным последствиям. Дефицит или избыток гормонов нарушают работу внутренних органов.
Основные гормоны, синтезируемые поджелудочной железой
Главный гормон, который способна секретировать поджелудочная железа – это инсулин. Он представляет собой полипептид, который включает в свой состав 51 аминокислоту. За его синтезирование отвечают бета-клетки, располагающиеся в панкреатических островках.
Гормон инсулин вырабатывается в поджелудочной железе, выполняет ряд функций. Он отвечает за регуляцию сахара в организме, способствует торможению синтеза глюкозы в печени, помогает снизить
Если нарушается такая «биохимия» в организме человека, то наблюдается рост сахара в крови, что увеличивает вероятность развития сахарного диабета в несколько раз.
Белковый гормон инсулин активизирует секрецию жирных кислот. Влияет на продуцирование веществ ЖКТ, гормонов роста и эстрогенов.
Помимо инсулина поджелудочная железа синтезирует следующие вещества:
- Гастрин.
- Амилин.
- Панкреатический полипептид.
- Глюкагон.
- С-пептид.
Липокаин может рассматриваться как второй гормон, вырабатываемый внутренним органом (помимо инсулина). Он тормозит развитие жировой инфильтрации печени, стимулирует липотропный обмен.
Функции гормональных веществ
Небольшое количество глюкозы всегда содержится в печени и мышцах, это является стратегическим запасом для организма человека. Этот запас представлен в виде гормона гликогена, который при надобности трансформируется в исходное состояние. Иными словами, преобразуется в глюкозу. Синтез гликогена происходит в печени, лейкоцитах и мышечной ткани. Гормон – главная форма существования углеводов в человеческом организме.
Глюкагон – еще одно вещество поджелудочной железы. Он помогает расщепляться гликогену, чтобы высвободилась глюкоза; способствует расщеплению липидов, вследствие чего в жировых клетках возрастает ферментированная липаза.
- Снижает концентрацию глюкагона.
- Замедляет выведение желудочного сока.
- Замедляет синтезирование соляной кислоты.
- Угнетает выработку панкреатических ферментов.
- Снижает объем крови в брюшной полости.
Панкреатический полипептид был выявлен сравнительно недавно. Влияние эндокринного гормона до конца не изучено.
Большинство ученых сходятся во мнении, что вещество способствует «экономии» пищеварительных панкреатических ферментов.
Уже много лет я изучаю проблему ДИАБЕТА. Страшно, когда столько людей умирают, а еще больше становятся инвалидами из-за сахарного диабета.
Спешу сообщить хорошую новость – Эндокринологическому научному центру РАМН удалось разработать лекарство полностью вылечивающее сахарный диабет. На данный момент эффективность данного препарата приближается к 100%.
Еще одна хорошая новость: Министерство Здравоохранения добилось принятия специальной программы, по которой компенсируется вся стоимость препарата. В России и странах СНГ диабетики до 6 июля могут получить средство – БЕСПЛАТНО!
Лабораторное исследование поджелудочной железы
Анализ на ферменты поджелудочной железы – это анализ крови, который обеспечивает выявление всех нарушений разнообразного патогенеза в работе и состоянии внутреннего органа. Он применяется для диагностики заболеваний поджелудочной железы.
В эндокринологии данное исследование имеет несколько показаний. Назначается при клинических симптомах болезней внутреннего органа, также рекомендуется при подозрении на гипофункцию или гиперфункцию поджелудочной железы.
Результаты обследования помогают оценить функциональность внутреннего органа, степень имеющихся повреждений; дифференцировать болезнь от других заболеваний. Кроме того, анализ рекомендуется для наблюдения за больными с хроническим панкреатитом, желчекаменной болезнью и др. недугами; выявить опухолевые новообразования в поджелудочной.
Анализ проводится для взрослого и ребенка. Особой подготовки не существует. Главное – нельзя курить за 30 минут до забора крови. В качестве биологического материала используется венозная жидкость.
Определяется содержание следующих показателей:
- С-пептид определяется с помощью ферментного исследования.
- Определение сахара в плазме крови.
- Липаза определяется колориметрическим способом.
- Амилаза общая в сыворотке крови, билирубин общий, патобиохимия холинэстеразы.
- С-реактивный белок.
Если по результатам расшифровки увеличена активность ферментов железы, возрос уровень реактивного белка, то это говорит об острой форме панкреатита. Патологический уровень сахара и С-пептида указывает на дисфункцию внутреннего органа.
Проверка поджелудочной железы назначается в следующих случаях:
- Подозрение на опухоль.
- При симптоматике вероятного поражения органа (боль в верхнем отделе живота, рвота, изменение цвета стула – эти симптомы могут свидетельствовать о серьезном нарушении, вплоть до расстройства всасывания питательных веществ в кишечнике).
- Если инструментальные методы диагностики показали структурные изменения внутреннего органа.
- При наличии наследственного фактора к патологиям органа.
- Профилактическое обследование.
Дополнительно могут назначаться другие исследования, например, гемотест, ультразвуковое исследование, компьютерная томография органов брюшной полости. Это необходимо для того чтобы исключить вероятные патологии других внутренних органов и систем, уточнить патогенез патологических процессов в организме. Итоги обследования анализируются с учетом симптомов, продолжительности патологии, сопутствующих недугов.
Гормоны, вырабатываемые поджелудочной, влияют на все аспекты жизнедеятельности человеческого организма. Они должны участвовать во многих процессах, чтобы поддерживать нормальную работу органов и систем. Все в организме взаимосвязано, поэтому немаловажное значение имеют и другие гормоны.
Тироксин вырабатывается щитовидной железой. Он воздействует на показатели артериальное давление человека, способствуя его повышению. Физиология, энергичность, подвижность также зависят от концентрации вещества в крови. Дефицит приводит к избыточному весу, постоянной усталости, ломкости волос и ногтей, пониженному давлению и пр. симптомам. Для лечения фармакология предлагает синтетические препараты, которые включают в свой состав искусственный тироксин.
Гормон адреналин вырабатывается в надпочечниках. При избытке вещества оказывается влияние на психическое и физическое состояние. При увеличении концентрации возрастает артериальное давление, что будет являться большим риском инфаркта, если в анамнезе проблемы с сердечно-сосудистой системой; резко понижается содержание сахара в организме.
Гормоны, которые синтезируются поджелудочной железой, необходимы для поддержания нормальной работы организма. Если наблюдается их дефицит или избыток, то требуется коррекция уровня веществ с помощью медикаментов и питания.
Информация о гормонах поджелудочной железы предоставлена в видео в этой статье.
Гормоны поджелудочной железы.
Поджелудочная железа синтезирует ферменты, необходимые для пищеварения. Эндокринная часть железы (островки Лан- геранса) секретирует по крайней мере четыре гормона: инсулин, глюкагон, сома- тостатин и панкреатический полипептид.
Структура и роль инсулина были рассмотрены выше. Глюкагон – 29-членный пептид, вызывающий повышение уровня глюкозы в крови за счет стимуляции расщепления гликогена в печени, увеличивает содержание глюкозо-6-фосфата в мышцах и обладает липолитическим (жирорасщепляющим) действием.
Эти гормоны высвобождаются в панкреатическую вену, впадающую в воротную вену печени, что имеет важное значение, поскольку для инсулина и глюкаго- на печень служит главной мишенью.
Основная роль инсулина и глюкагона сводится к регуляции углеводного обмена, однако гормоны поджелудочной железы оказывают влияние и на многие другие процессы. Например, соматостатин подавляет секрецию гормона роста. Он участвует в локальной регуляции секреции инсулина и глюкагона.
На рис. 12.15 приведена схема регулирования содержания глюкозы СН в плазме крови человека.
В соответствии с этой схемой мозг (Сг), поджелудочная железа (Рп), печень (Нр) и другие ткани (Т1) находятся в потоке крови, через который осуществляется гуморальная связь между различными органами. Схема отражает одну из специфических особенностей взаимосвязи метаболических путей в организме – пространственное разделение взаимодействующих компонентов.
Большинство химических превращений в организме, а также активный транспорт через клеточные мембраны осуществляются с помощью ферментов и белковых молекул (Е).
В схеме рис. 12.15 учтены только два гормона, синтезируемые в поджелудочной железе, – инсулин (In) и глюкагон (G1).
Реакции в поджелудочной железе:
Реакции в печени:
Реакции в тканях:
Реакции в крови (дезактивация гормонов):
В приведенных здесь реакциях Е,, Еь, Еа, Ер – ферменты, функционирующие в соответствующих органах или тканях; Рг – протеин; In, G1 – гормоны инсулин и глюкагон; СН, СН, – глюкоза в крови и тканях, Gn – гликоген со степенью полимеризации и; Xj, Хс, – продукты дезактивации гормонов.
Рис. 12.15. Схема регу лирования концентрации глюкозы СН в крови человека:
Сг – мозг. Рп – поджелудочная железа, Нр – печень. TI – ткани. In – инсулин. GI – глюкагон. Ев. Е* – ферменты поджелудочной железы, Еь – гликогснфосфорилаза, 1ц – фермент тканей, Оь – гликоген печени.
СН, – глюкоза тканей
Роль инсулина и глюкагона в жизнедеятельности организма хорошо изучена. Инсулин активирует фермент Et и ускоряет переход глюкозы в ткани скелетных мышц и жировую ткань. В результате такой активации уровень глюкозы в крови быстро падает. Глюкагон активирует фермент Еь – гликогенфосфорилазу – и ускоряет процесс деполимеризации полисахарида гликогена в печени и мышцах с отщеплением глюкозы. В результате концентрация глюкозы в крови возрастает.
Увеличение содержания глюкозы в крови является стимулом для клеток поджелудочной железы к увеличению активности фермента Ер, что приводит к активации секреции инсулина. Уменьшение содержания глюкозы в крови приводит к активации фермента Еа в а-клетках этой железы и увеличению секреции глюкагона.
На рис. 12.16 приведен типичный пример автоколебательного характера уменьшения содержания глюкозы в крови человека после перорального введения различных доз этого вещества.
Рис. 12.16. Изменение концентрации глюкозы с (мг/100 мл) от времени в крови здорового человека после перорального приема внутрь:
/ – 25 и 2- 100 г глюкозы (норма 70-110 мг/100 мл (4-6 мМ))
Схему регулирования уровня глюкозы в крови нетрудно описать с помощью кинетических уравнений. Анализ этих уравнений позволяет сделать вывод, что автоколебательный характер возвращения биохимического состава организма к исходному состоянию после импульсного возмущения связан с наличием по крайней мере одной автокаталитичсской реакции в метаболическом пути. Такие реакции имеются в рассмотренной здесь схеме реакций регулирования уровня сахара в крови.
Например, увеличение концентрации глюкозы в соответствии с реакцией Ер+ СН Ер-СН -> Ер+ In приводит к увеличению содержания инсулина в крови,
а это вызывает увеличение абсорбции глюкозы тканями мышц
(Е,+ In Et-In + СН E,-In + СН E, In + СН,).
Помимо автоколебаний следует обратить внимание на другие особенности регулирования сахара, которые иллюстрирует рис. 12.16.
Во-первых, максимальное количество глюкозы в крови возрастает непропорционально дозе: дозы различаются в 4 раза, максимальные количества – примерно лишь в 1,5 раза. Эти максимальные значения в несколько раз ниже предельно возможных при данных дозах 25 и 100 г. Максимальное значение при меньшей дозе достигается значительно быстрее, чем при большой. Кроме того, наблюдается «проскакивание» исходного количества глюкозы в крови к концу периода релаксации до стационарного значения.
Перечисленные особенности адаптационного регулирования в той или иной мере проявляются и для других биогенных веществ, вводимых в организм. Они связаны с характером всасывания или введения в кровь, с одной стороны, и характером реакционной цепи превращений – с другой. Практическое отсутствие периода задержки указывает на быстрое включение компенсационного механизма адаптации внутренней среды.
Экспериментальное исследование регулирования концентраций ионов ОН , CI , аминокислот и других веществ в организме показывает, что регулирование и этих компонентов носит автоколебательный характер. Это общее свойство процессов регулирования уровня различных веществ в крови, очевидно, отражает общность механизмов регулирования, в основе которых лежат реакционные цепи типа схемы регулирования уровня глюкозы.
Приведенные выше факты позволяют сделать заключение, что регулирование температуры тела также должно демонстрировать автоколебательный характер достижения равновесного значения. Этот вывод подтверждается экспериментальными данными.
Изменение температуры в организме гомойотермных (теплокровных) животных вызывает соответствующую реакцию терморецепторов. Охлаждение тканей приводит к увеличению расхода энергии для поддержания температуры на необходимом уровне, что, в свою очередь, интенсифицирует процессы поглощения глюкозы тканями и соответствующее уменьшение концентрации глюкозы в крови. В результате включается механизм компенсации, отображаемый реакциями регулирования уровня глюкозы.