Признаки патологии пбс что это
Лечение в Италии
(925) 50 254 50
Первичный боковой склероз – лечение в Италии
Первичный боковой склероз – дегенеративное заболевание нервной системы: вариант болезни двигательных нейронов, при котором поражаются только центральные (корковые) двигательные нейроны и пирамидные тракты (в боковых столбах спинного мозга). Проявляется относительно быстро прогрессирующим спастическим тетрапарезом или нижним парапарезом. В отличие от бокового амиотрофического склероза, отсутствуют клинические или электромиографические признаки поражения периферических двигательных нейронов передних рогов спинного мозга (фасцикуляции, атрофии мышц и т.д.). Лечение симптоматическое.
Первичный латеральный склероз может развиться в любом возрасте, но обычно возникает в возрасте от 40 до 60 лет. Один из подвидов первичного латерального склероз – ювенильный первичный латеральный склероз – начинается в раннем детстве и вызывается унаследованием патологического гена от родителей.
Первичный латеральный склероз часто принимают за другое, более распространенное заболевание двигательного нейрона – амиотрофический латеральный склероз (АЛС). Однако первичный латеральный склероз прогрессирует медленнее, чем АЛС, и в большинстве случаев не ведет ксмерти.
Признаки и симптомы первичного латерального склероза (ПЛС) обычно развиваются в течение нескольких лет. К ним относятся:
- Ригидность, слабость и спастичность нижних конечностей
- По мере ослабления мышц нижней конечности – спотыкание, трудности с поддержанием равновесия и неуклюжесть
- Слабость и ригидность, распространяющиеся на мышцы туловища, затем верхних конечностей, кистей, языка и челюсти
- По мере ослабления мышц лица – охриплость, снижение скорости речи, невнятная речь и слюнотечение
- На поздних стадиях заболевания – трудности при глотании и дыхании
- ПЛС встречается реже и начинается в языке или кистях и затем распространяется по спинному мозгу в нижние конечности.
В среднем первичный латеральный склероз (ПЛС или ПБС) протекает примерное в течение 20 лет, однако у разных людей заболевание может иметь крайне разные последствия. В некоторых случаях сохраняется способность к ходьбе, однако в других может возникнуть потребность в инвалидной коляске или других вспомогательных средствах.
Как известно, нейронная ткань центральной (головной и спинной мозг) и периферической нервной системы выполняет в организме ключевые аналитические, контрольные и регуляторные функции. Будучи эволюционно молодой (особенно это касается неокортекса, «новой коры» головного мозга), нейронная ткань является высокоорганизованной живой материей и отличается сложнейшей структурой перекрестных взаимосвязей.
Любой нейродегенеративный или атрофический процесс (атрофия – уменьшение в объеме, «исчезновение» ткани вследствие прекращения ее питания) представляет собой патологию серьезную, тяжелую и, как правило, прогностически неблагоприятную. Почти все заболевания этой группы, к счастью, достаточно редки; многие из них носят наследственный характер.
Отдельную подгруппу образуют процессы т.н. нейромышечной дегенерации, поражающие преимущественно моторные (двигательные) нейроны. Трагическая и героическая судьба выдающегося физика С.Хокинга сделала широко известным, в частности, боковой амиотрофический склероз (БАС).
Действительно, на долю этого диагноза приходится до 80% всех случаев нейромышечной дегенерации, далее идут прогрессирующие бульбарный паралич (ок. 10%) и мышечная атрофия (ок. 8%). И лишь 2% приходится на т.н. первичный боковой (латеральный) склероз (ПБС; иногда можно встретить также аббревиатуры ПЛС или PLS). Учитывая редкость нейродегенеративных процессов вообще, ПБС считается исключительно редким заболеванием. Впрочем, статистические данные о частоте встречаемости недостаточны.
Предполагается, что ПЛС у взрослых не сокращает продолжительность жизни, однако по мере ослабления мышц может постепенно снижать качество жизни. Слабость мышц повышает частоту падений, что может привести к травмам.
Этиопатогенетическое и, вообще, сколько-нибудь эффективное лечение к настоящему времени находится в стадии разработки. Проводится паллиативная (симптоматическая) терапия, включая медикаментозные средства укрепления мышц, физиотерапевтические процедуры, ЛФК. С определенного момента больные нуждаются в социальном обеспечении, постоянном обслуживающем уходе и опеке.
! Несмотря на то, что многие из описанных в данном разделе болезней считаются неизлечимыми, в Центре лечения редких заболеваний в Милане постоянно ведется поиск новых методов. Благодаря генной терапии удалось добиться выдающихся результатов и полностью излечить некоторые редкие синдромы.
Обратитесь к консультанту на сайте или оставьте заявку – так вы можете узнать, какие методы предлагают итальянские врачи. Возможно, данное заболевание уже научились лечить в Милане.
Первичный боковой склероз
- мозг
- позвоночник
- нервы и сосуды
1. Общие сведения
В общественном сознании слово «склероз» ассоциируется почти исключительно со слабой памятью; причинно-следственная связь действительно имеется, хотя и не прямая. В строгом медицинском понимании термин «склероз» означает процесс дегенерации какой-либо функциональной, специализированной ткани (сосудистых стенок, паренхимы легких, печени, простаты и пр.), т.е. ее перерождения в более плотную и объемную соединительную (рубцовую) ткань. Для обозначения относительно слабого склеротического процесса нередко употребляется очень близкий синоним «фиброз»; тотальные катастрофические варианты называют «циррозом». Сути, однако, это не меняет: склероз любого типа приводит к тому, что пораженный орган или целая система все хуже справляется со своими природными функциями и постепенно превращается, фактически, в бесполезный придаток.
Как известно, нейронная ткань центральной (головной и спинной мозг) и периферической нервной системы выполняет в организме ключевые аналитические, контрольные и регуляторные функции. Будучи эволюционно молодой (особенно это касается неокортекса, «новой коры» головного мозга), нейронная ткань является высокоорганизованной живой материей и отличается сложнейшей структурой перекрестных взаимосвязей. Любой нейродегенеративный или атрофический процесс (атрофия – уменьшение в объеме, «исчезновение» ткани вследствие прекращения ее питания) представляет собой патологию серьезную, тяжелую и, как правило, прогностически неблагоприятную. Почти все заболевания этой группы, к счастью, достаточно редки; многие из них носят наследственный характер.
Отдельную подгруппу образуют процессы т.н. нейромышечной дегенерации, поражающие преимущественно моторные (двигательные) нейроны. Трагическая и героическая судьба выдающегося физика С.Хокинга сделала широко известным, в частности, боковой амиотрофический склероз (БАС). Действительно, на долю этого диагноза приходится до 80% всех случаев нейромышечной дегенерации, далее идут прогрессирующие бульбарный паралич (ок. 10%) и мышечная атрофия (ок. 8%). И лишь 2% приходится на т.н. первичный боковой (латеральный) склероз (ПБС; иногда можно встретить также аббревиатуры ПЛС или PLS). Учитывая редкость нейродегенеративных процессов вообще, ПБС считается исключительно редким заболеванием. Впрочем, статистические данные о частоте встречаемости недостаточны.
2. Причины
Триггерные (запускающие) факторы ПБС, как и факторы риска, на сегодняшний день в точности не установлены. В частности, предпринимаемые попытки связать заболеваемость первичным боковым склерозом с генетическим, семейным анамнезом также пока не приносят достаточно достоверных и аргументированных результатов.
3. Симптоматика, диагностика
Специфическим отличием ПБС от других аналогичных нейродегенеративных процессов является исключительное поражение центральных (корковых) моторных нейронов при сохранности периферических. При ПБС не наблюдаются мышечная атрофия, выпадение чувствительности и некоторые другие расстройства, присущие заболеваниям близкой природы.
Первичный боковой склероз начинается обычно в зрелом возрасте (интервал 40-50 лет) и манифестирует мышечной ригидностью (жесткостью, неконтролируемым напряжением), нарушениями речи и пищевого акта (жевание, глотание). Нарушаются координация произвольных движений, походка, мелкая пальцевая моторика (напр., почерк); возможна аффективная неустойчивость и неадекватность (приступы смеха или плача, не соответствующие ситуации), в редких случаях – сфинктерная дисфункция. Заболевание неуклонно прогрессирует, приводя в итоге к т.н. спастическому параличу с невозможностью самостоятельного приема пищи и, вообще, самообслуживания.
ПБС считается заболеванием со значительно менее злокачественным течением, чем при боковом амиотрофическом или прогрессирующем бульбарном склерозе, прогрессирующей мышечной атрофии. Средняя продолжительность жизни после манифестации симптоматики ПБС составляет, по некоторым оценкам, до 10 лет и более. Однако встречаются и значительно более быстрые темпы нарастания двигательной несостоятельности.
Вообще, неточность и противоречивость медико-статистических данных, накопленных в отношении ПБС, во многом объясняется значительными трудностями диагностики и отсутствием каких-либо узконаправленных методов подтверждающего и дифференцирующего обследования. Выраженное сходство симптоматики, особенно на ранних стадиях, приводит к ошибочной диагностике БАС, демиелинизирующих заболеваний, вирусной миелопатии и пр., что негативно отражается на точности эпидемиологической статистики и по ПБС, и по неверно диагностированным заболеваниям.
Необходимо тщательное изучение анамнеза, специфики клинической картины, динамики прогрессирования нейромышечных нарушений. Назначаются МРТ и электронейромиографические исследования; функциональное состояние внутренних органов, могущих страдать при ПБС, контролируется лабораторными клиническими анализами.
4. Лечение
Этиопатогенетическое и, вообще, сколько-нибудь эффективное лечение к настоящему времени не разработано. Проводится паллиативная (симптоматическая) терапия, включая медикаментозные средства укрепления мышц, физиотерапевтические процедуры, ЛФК. С определенного момента больные нуждаются в социальном обеспечении, постоянном обслуживающем уходе и опеке.
Проявления и лечение первичного бокового склероза
Содержание:
Частота патологии составляет 2 – 5 человек на 100 тысяч населения. Чаще всего первые симптомы появляются в возрасте 50 – 60 лет, хотя иногда могут встречаться и в более молодом возрасте. Продолжительность жизни от начала заболевания до смерти составляет от 1 до 4 лет.
Какие области поражаются
Патология развивается постепенно, поэтому симптомы проявляются далеко не все и не сразу. Постепенно нарушается глотание, появляются проблемы с дыханием, движением. Со временем поражённые области могут затрагивать практически всё тело.
Кисти и руки поражаются быстрее всего. Даже при таких простых действиях, как мытьё посуды или помешивание в кружке сахара могут возникать значительные затруднения. Со временем сила в руках практически полностью исчезает, а в ладонях и пальцах появляется сильная слабость.
Из-за ослабления ног передвигаться будет всё сложнее и сложнее. При поражении зон, которые отвечают за эмоции, пациент может непроизвольно смеяться или плакать. Из-за ослабленных мышц грудной клетки и шеи дыхание становится сильно затруднённым. Также патология сказывается и глотании, и на речи, что вызывает проблемы с питьём и едой.
При этом не происходит нарушений интеллекта, а также в норме остаётся зрение, вкус, обоняние и осязание.
Причины
Первичный боковой склероз – заболевание, которое появляется по самым разным причинам, однако уже доказано, что это генетическая патология, которая начинается при нарушении в хромосомах.
В 10% всех случаев болезнь передаётся по наследству, причём родители могут и не иметь явных её признаков. Ещё 25% — это случайные мутации генов, которые происходят по тем или иным причинам. Не следует считать, что заболевание появляется при инфицировании организма матери или плода тем или иным вирусом.
Заболевание протекает очень быстро и за первый год своего развития разрушается примерно 80% всех мотонейронов, что не позволяет провести лечение в полном объёме.
Но всё же в большинстве случаев причина развития заболевания остаётся невыясненной. Точно узнать, почему оно появляется, невозможно. При исследовании были высказаны предположения о том, что первичный боковой склероз может появиться в результате влияния тех или иных химических веществ, травм, стрессовых ситуаций высоких нагрузок, особенно у спортсменов.
Некоторые формы
Симптомы первичного бокового склероза можно разделить на несколько форм. Первая и самая частая – спастическая параплегия. Это выражается в повышенном спастическом тонусе ног, что приводит к нарушению походки. Такое состояние является результатом генетической мутации.
При спинальной мышечной атрофии появляется слабость и уменьшение мышечной массы в размерах. Также здесь наступает полное отсутствие иннервации нервными волокнами. В зависимости от появившихся симптомов и от времени их развития бывает несколько вариантов течения этого заболевания.
Также одним из вариантов первичного бокового склероза следует считать детский церебральный паралич или последствия полиомиелита.
Возможное лечение
Назначаются антиоксидантные препараты, креатин, карнитин, витамины. Есть лекарство Рилузол, но официально на территории РФ оно запрещено.
Для устранения спазма и боли используется карбамазепин, при сильном мышечном тонусе – миорелаксанты, а точнее — сирдалуд и баклофен. При затруднении дыхания проводится перевод на искусственную вентиляцию лёгких.
Прогноз всегда неблагоприятный. Смерть наступает в течение первых 4 лет от начала заболевания, а иногда и в первый год от момент постановки диагноза.
Также нет никакой профилактики развития патологии, так как точно не понятно, что вызывает её появление. При планировании беременности семьям, в роду которых были родственники с данными болезнями, следует обязательно пройти генетическую консультацию и установить риск рождения больного ребёнка.
Косвенные признаки патологий панкреато-билиарной системы
Все органы пищеварения связаны между собой, и при наличии воспаления в одном из них возникают проблемы в другом. Застой желчи на фоне заболеваний печени, холецистита, холангита приводит к развитию панкреатита.
Раннее выявление болезни помогает своевременно начать лечение и предупредить необратимые изменения в тканях. Поэтому важно знать, какие существуют косвенные признаки патологии панкреато-билиарной системы, и при их появлении сразу обратиться к врачу.
Причины развития заболеваний
Панкреато-билиарная система состоит из нескольких взаимосвязанных органов, расположенных в брюшной полости и отвечающих за нормальное пищеварение. Любое отклонение в работе одного из них немедленно сказывается на состоянии другого. Чаще всего наблюдается билиарный панкреатит.
Это вторичный процесс, возникающий из-за:
- желчнокаменной болезни, так как резкая закупорка провоцирует появление острого билиарного панкреатита;
- цирротических изменений гепатоцитов;
- холангита (воспаления желчевыводящих протоков);
- холецистита (поражения желчного пузыря);
- кист и новообразований в тканях печени и желчевыводящих путей.
Патологии панкреато-билиарной зоны появляются в силу следующих причин:
- инфицирование желчных путей с попаданием патогенов в поджелудочную железу с током лимфатической жидкости;
- нарушение образования и выведения желчи, ее застой;
- поражение печени (цирроз, рак);
- патология фатерова сосочка;
- неправильное питание, голодание;
- прием ряда лекарственных средств;
- врожденные отклонения в структуре протоков и желчных путей;
- резкое похудение.
Важно! Панкреато-билиарная дисфункция часто развивается при формировании сладжа (множества мелких конкрементов), когда происходит нарушение физико-химических свойств желчи с последующим выпадением осадка. Песок и небольшие камни травмируют слизистую, вызывая сужение протоков.
Диагностика
Для уточнения диагноза используются лабораторные и инструментальные методы исследования:
- В общем и биохимическом анализе крови и мочи будут видны признаки воспалительного процесса. Отмечается повышение билирубина, щелочной фосфатазы, сывороточной амилазы.
- Копрограмма укажет на присутствие в каловых массах непереваренной пищи (волокон, крахмала, жира).
- Важным диагностическим методом при данной патологии считается УЗИ. С его помощью определяется наличие камней, опухоли кисты в гепатобилиарной системе, анатомо-физиологические особенности органов брюшной полости.
- Более информативный способ – КТ с использованием контраста. Его проводят для уточнения состояния желчных протоков.
- Дополнительную картину помогают получить эндоскопические исследования: ретроградная и магнитно-резонансная холангиопанкреатография.
Симптоматика
Признаки патологии не являются специфическими и могут напоминать другие заболевания органов пищеварения:
- Выраженный болевой синдром. Локализация боли вариабельна, пациент указывает на эпигастрий, правое или левое подреберье. При заболевании поджелудочной железы она может носить опоясывающий характер.
- Острая боль возникает через 1,5-2 часа после приема пищи. Чаще всего неприятные ощущения связаны с нарушением диеты и приемом жирной, жареной, копченой или острой пищи. В некоторых случаях боль появляется сразу после употребления газированных напитков в результате спазма сфинктера Одди в фатеровом сосочке.
- Одновременно с приступом отмечаются лихорадка, тошнота, рвота, горькая отрыжка.
- Желтуха развивается в результате закупорки желчевыводящих путей камнем или опухолью. Перекрытие фатерова сосочка способствует развитию билиарного панкреатита.
- Когда в патологический процесс вовлекаются ткани поджелудочной железы, нарушаются ее функции. Поражение островков Лангерганса приводит к снижению продукции инсулина и увеличению глюкозы в крови. Хронический процесс с полным поражением бета-клеток – основная причина сахарного диабета I типа.
- Экзокринные отклонения в работе поджелудочной проявляются в виде расстройства кишечника с частой дефекацией. Стул становится неоформленным, жидким, зловонным и приобретает жирный блеск. У пациента наблюдаются диспепсия, снижение аппетита, повышенное газообразование в кишечнике.
- Симптомы билиарного панкреатита ничем не отличаются от признаков воспаления железы, но к ним присоединяются повышение билирубина в крови, пожелтение кожных покровов и слизистых.
Важно! При появлении подобных признаков необходимо провести дифференциальную диагностику с язвой, опухолью органов брюшной полости, гастритом, вирусным поражением печени. Для этого и существуют инструментальные методы и лабораторные анализы.
Оказание помощи
Лечение патологии зависит от степени запущенности процесса и причины появления. Если ей выступает камень, перекрывающий протоки, единственным методом будет оперативное удаление. Таким же способом исправляется нарушение структуры фатерова сосочка.
Консервативная терапия
Медикаментозное лечение включает в себя заместительную терапию при экзо- или эндокринной недостаточности поджелудочной, а также применяются препараты для купирования негативной симптоматики:
- Повышение уровня глюкозы при нарушении функции или структуры бета-клеток требует использования инсулина. Препарат вводится парентерально.
- Ферменты используются, когда их недостаток приводит к нарушению процесса переваривания пищи.
- Если в крови повышается билирубин, то проводится детоксикация организма солевыми растворами.
- Профилактика присоединения инфекции осуществляется с помощью антибактериальной терапии.
- Боль купируется спазмолитиками.
- При быстром повреждении железы происходит выброс ферментов и других активных веществ, которые могут разрушить орган. Чтобы этого не произошло, используются средства для угнетения выделения желудочного сока.
- При отклонениях, связанных с гепатобилиарной системой, лечение обязательно включает в себя диету. Питаться следует теплой пищей и маленькими порциями до 4-5 раз в сутки.
Заключение
Любые изменения в работе органов, входящих в панкреато-билиарную систему, могут привести к разладу обменных процессов, нарушению сахарного обмена, желтухе. При возникновении первых признаков заболевания нужно обратиться к врачу для постановки точного диагноза и немедленно начинать лечение.
Боковой амиотрофический склероз (болезнь Шарко, Герига). тяжёлое неизлечимое прогрессирующее заболевание.
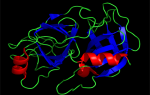
Настоящее фото мотонейрона (двигательного нейрона в передних рогах спинного мозга) – закупорка межсинаптических щелей (зелёные точки) – блокада передачи импульсов через медиаторы (вещества для передачи импульсов) в синапсы (места соединения) отростков нервных клеток.
В центре – тело мотонейрона.
Красные линии -длинные отростки мотонейрона – аксоны и короткие -дендриты.
Причина появления блокады передачи импульсов в межсинаптических щелях учёными мира не найдена. Предположительно – мутация гена,кодирующего фермент передачи этих импульсов через нейромедиаторы – супероксиддисмутазы. (СОД).
Предрасположенность к мутациям гена может иметь наследственный характер по аутосомно-рецессивному типу.
Эндемические (массовые вспышки) случаи этого заболевания зафиксированы у групп военных, живущих в островах на тихом океане. Чаще болеют мужчины от 40 до 60 лет.Следовательно не исключается инфекционная причина развития заболевания.
Боковой амиотрофический склероз. (БАС)..
Показано истончение нервных волокон в случае БАС и нарушение иннервации (передачи нервных импульсов) к мышцам. Как следствие – уменьшение работы мышцы и её последующая атрофия. (уменьшение размеров, обратное развитие.)
Блокада передачи нервных импульсов к мышцам (как к поперечно-полосатым которыми мы управляем сами своей волей так и к к гладким, работающим, независимо от нашего сознания, усилий и воли) пищеварительной и дыхательной системы ведёт к смерти из-за невозможности совершать эти жизненно важные моменты работы мускулатуры.
Две статьи из медицинских источников:
1) Теория аксостаза бокового амиотрофического склероза. Аксональная теория бокового амиотрофического склероза
Теория аксостаза основана на анализе патологических процессов, происходящих в аксональном транспорте мотонейронов [Chou S., 1992]. Наибольшими нейронами организма являются двигательные мотонейроны передних рогов спинного мозга и пирамвды Беца. Они должны поддерживать интеграцию дендритов, часто протяженностью более 1 см, и аксон, достигающий 100 см. В аксоне имеются непрерывные потоки, через которые клеточное тело направляет структурные и функциональные белки на периферию и получает обратные сигналы. Ортоградный транспорт бывает 2 видов: а) быстрый — 400 мм в день, идущий в обоих направлениях и транспортирующий связанные с мембраной белки и гликопротеиды, б) медленный — несколько миллиметров в день, транспортирующий сети микрофиламентов, микротрубочек, нейрофиламентов, как компонент “а” (0,1—2 мм в день), а также большой комплекс растворимых белков, как компонент “б” (2—4 мм в день). Ретроградный аксональный транспорт несет эндогенные (аминокислоты, фактор роста нервов) и экзогенные (токсин столбняка, вирус полиомиелита, простого герпеса, бешенства, лектин пероксидазы хрена и др.) субстанции от терминальных аксонов к клеточному телу со скоростью свыше 75 мм в день. Морфологические исследования аксонального транспорта в биоптатах двигательных веточек периферических нервов больных боковым амиотрофическим склерозом выявили уменьшение скорости ретроградного аксонального транспорта и, следовательно, связи терминального аксона с перикарионом [Bieuer A. et al., 1987]. В межреберных нервах больных АБС еще до развития признаков нейрональной дегенерации появляются изменения белков микротрубочек [Binet S. et al., 1988].
Улыраструктурные исследования проксимального аксона и аксонального бугорка мотонейронов переднего рога спинного мозга больных, умерших от бокового амиотрофического склероза [Sasaki S. et al., 1996], показали нарушение быстрого аксонального транспорта. Гладкий эндо-плазматический ретикулум теряет структуру: происходит скопление митохондрий, лизосом, Леви-подобных телец, эозино-фильных и гиалиновых включений, липофусциновых гранул, особенно в аксональном бугорке. Присутствие этих необычных структур является отражением дисфункции аксонального транспорта. Применительно к возможной этиологии АБС еще ранее выдвинута концепция “аксостаза” [Chou S., 1992]. Ней-ротоксические факторы путем ретроградного транспорта избирательно поражают нейрон, создавая феномен “суицидцального транспорта”. Ухудшение медленного транспорта в аксоне сопровождается скоплением нейрофиламентов, набуханием проксимального аксона и последующей дистальнои аксональной атрофией, а также вторичной демиелинизацией, характерной для центральной дистальнои аксонопатии или “ретроградного умирания” — “dying back”. Определенную значимость в развитии ранних морфологических изменений мотонейронов при АБС имеет теория аутоиммунитета [Smith R. et al., 1996], основанная на появлении антител к зарядам входа кальциевых каналов. Пассивный перенос фракций, содержащих иммуноглобулин, мышам вызывает изменения нервно-мышечных соединений, сходные с таковыми при спорадическом АБС. У животных эти изменения отражают расстройства внутриклеточного Са2+ гомеостаза, и раннее повреждение пластинчатого комплекса в мотонейронах в форме набухания и фрагментации. Иммуноглобулины от больных спорадическим боковым амиотрофическим склерозом вызывают зависимый от Са2+ апоптоз клеток вследствие оксидативных повреждений. Апоптоз, обусловленный иммуноглобулином от указанных больных, регулируется присутствием связанных белков, которые могут модулировать избирательную ранимость нейронов при спорадическом АБС.
2) Боковой амиотрофический склероз
БОКОВОЙ АМИОТРОФИЧЕСКИЙ СКЛЕРОЗ (БАС, «болезнь Шарко», “болезнь Герига”, «болезнь двигательных нейронов») – идиопатическое нейродегенеративное прогрессирующее заболевание неизвестной этиологии, обусловленное избирательным поражением периферических двигательных нейронов передних рогов спинного мозга и двигательных ядер ствола мозга, а также корковых (центральных) мотонейронов и боковых столбов спинного мозга.
Несмотря на более чем 100-летнее изучение, боковой амиотрофический склероз (БАС) остается фатальным заболеванием центральной нервной системы. Заболевание характеризуется неуклонно прогрессирующим течением с избирательным поражением верхнего и нижнего мотонейронов, что приводит к развитию амиотрофий, параличей и спастичности. До настоящего времени вопросы этиологии и патогенеза остаются невыясненными, в связи с чем не разработаны специфические методы диагностики и лечения этого заболевания. Рядом авторов отмечено повышение частоты встречаемости заболевания среди лиц молодого возраста (до 40 лет).
МКБ-10 G12.2 Болезнь двигательного неврона
Боковой амиотрофический склероз дебютирует в возрасте 40 – 60 лет. Средний возраст начала заболевания 56 лет. БАС – болезнь взрослых, и не наблюдается у лиц моложе 16 лет. Несколько чаще заболевают мужчины (отношение мужчины-женщины 1,6-3.0: 1).
БАС является спорадическим заболеванием и встречается с частотой 1,5 – 5 случая на 100 000 населения.
В 90% случаев БАС носит спорадический, а в 10% – семейный или наследственный характер как с аутосомно-доминантным (преимущественно), так и с аутосомно-рецессивным типами наследования. Клинические и патоморфологические характеристики семейного и спорадического БАС практически идентичны.
В настоящее время возраст является основным фактором риска при БАС, что подтверждается нарастанием заболеваемости после 55 лет, и в этой возрастной группе уже не наблюдается различий между мужчинами и женщинами. Несмотря на достоверную связь БАС с возрастом, старение является только одним из предрасполагающих факторов развития патологического процесса. Вариабельность заболевания как в различных возрастных группах, так и среди лиц одного возраста предполагает существование определённых факторов риска: дефицит, или наоборот, наличие определённых нейропротективных факторов, к которым в настоящее время относят: нейростероиды или половые гормоны; нейротрофические факторы; антиоксиданты.
Некоторые исследователи отмечают особо благоприятное течение заболевания у молодых женщин, что подтверждает несомненную роль половых гормонов, в особенности эстрадиола и прогестина, в патогенезе бокового амиотрофического склероза. Подтверждением этому являются: большая частота встречаемости БАС у мужчин до 55 лет (при этом у них отмечается более раннее начало и быстрое прогрессирование заболевания по сравнению с женщинами); с наступлением менопаузы женщины болеют также часто, как и мужчины; единичные случаи заболевания боковым амиотрофическим склерозом во время беременности. К настоящему времени существуют единичные работы по изучению гормонального статуса больных с боковым амиотрофическим склерозом, и ни одной, посвящённой определению концентраций гормонов у молодых пациентов.
Этиология заболевания не ясна. Обсуждается роль вирусов, иммунологических и метаболических нарушений.
В развитии семейной формы БАС показана роль мутации в гене супероксиддисмутазы-1 (Cu/Zn-супероксиддисмутазу, SOD1), 21q22-1 хромосома, выявлен также БАС, связанный с 2q33-q35 хромосомой.
Синдромы, клинически не отличимые от классического БАС, могут возникать в результате:
•опухоли большого затылочного отверстия
•спондилез шейного отдела позвоночника
•артериовенозная аномалия спинного мозга
•бактериальные – столбняк, болезнь Лайма
•вирусные – полиомиелит, опоясывающий лишай
Интоксикации, физические агенты:
•токсины – свинец, алюминий, другие металлы.